[本站讯]近日,化学与化工学院前沿化学研究院李兴伟教授团队在铑催化烯烃不对称远程氢胺化反应方面取得新进展,相关成果以“Asymmetric Vicinal and Remote Hydroamination of Olefins by Employing a Heck-Reaction Derived Hydride Source”为题,发表在国际期刊J. Am. Chem. Soc.(中科院一区,TOP, IF=14.4)。山东大学博士后米瑞杰为第一作者,李兴伟教授为通讯作者,山东大学为第一完成单位。
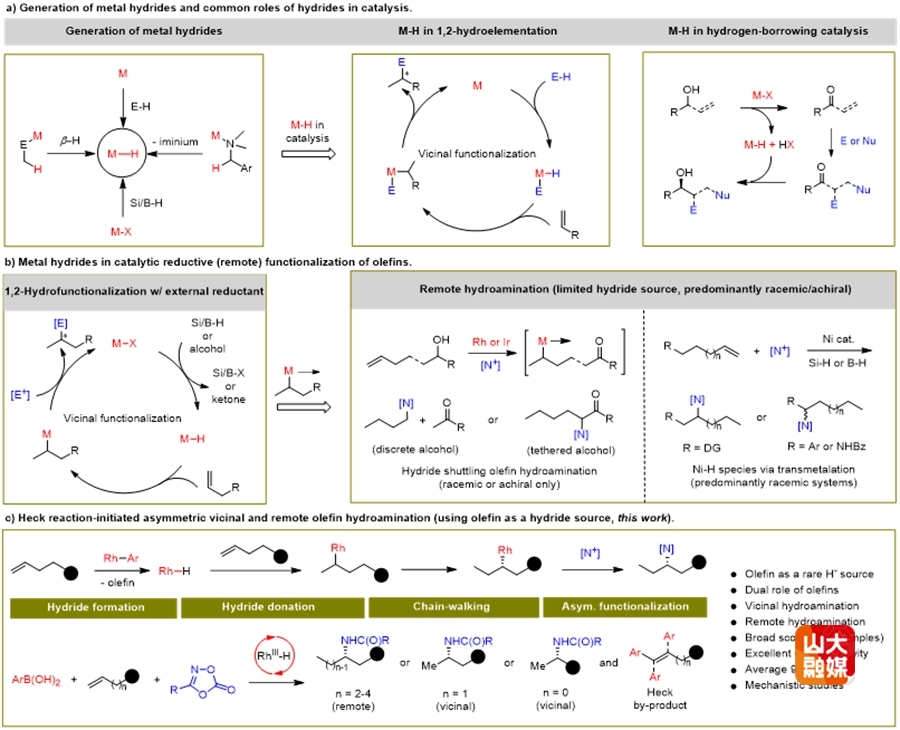
图1 铑催化烯烃不对称氢胺化反应研究
氢氨化反应是一种能高效构建手性胺骨架的经济性良好的方法,在不对称合成反应中应用广泛。在目前研究报道中的氢源大多来自于酸、醇、硼氢、以及硅氢等有机分子,因此开发新型的氢来源对于氢官能化反应的发展至关重要。基于以上背景,李兴伟课题组报道了一种铑催化的烯烃不对称氢胺化反应,在温和条件下,以优异的对映选择性,合成了一系列不同链长的α-和β-氨基酰胺(图1)。
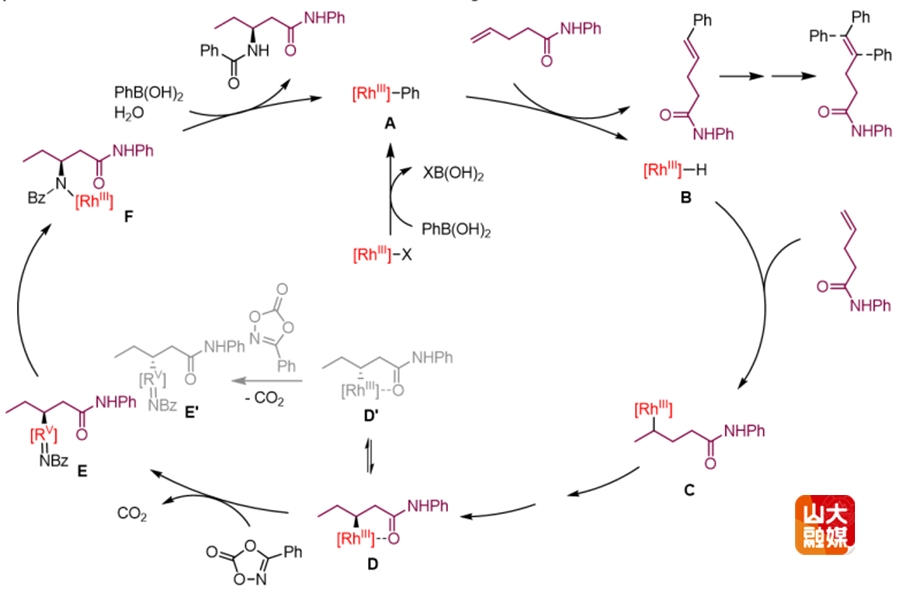
图2 反应的机理
该方法的亮点:1.创新的氢源利用:利用烯烃作为氢源,通过Heck反应原位生成铑氢中间体,避免了外部氢源的局限性,为金属氢化物在C-N键形成反应中的应用开辟了新途径。2.区域选择性精准调控:短链烯烃倾向于1,2-氢胺化,生成α-氨基酰胺;长链烯烃通过链行走机制实现1,3-或1,4-远程氢胺化,生成β-氨基酰胺。3.深入的机理研究:氘代标记实验支持Heck反应先发生生成铑氢中间体,且该中间体插入烯烃过程可逆的推断。动力学同位素效应和Hammett关联研究表明,二恶唑酮的配位-脱羧为决速步,且富电子的二恶唑酮更易与金属中心结合,后续形成铑氮宾的步骤是立体决定步骤(图2)。

此项研究成果不仅扩展了不对称催化领域的研究范畴,也为手性氨基酰胺类化合物的高效合成提供了新的方法和策略,具有潜在的工业和药物开发应用价值。上述工作得到国家自然科学基金委以及山东大学双一流建设经费的资助。