[本站讯]近日,基础医学院马春红教授和李春阳副教授作为共同通讯作者在国际权威期刊Journal of Hepatology(5年IF=28.1)发表题为“Tim-3 facilitates dendritic cell ferroptosis and impairs anti-tumor immunity in steatohepatitis-related HCC”的研究论文。该研究揭示了在高脂微环境中免疫检查点分子Tim-3促进代谢功能障碍相关脂肪性肝病(MASLD)相关肝细胞癌(HCC)进展的新机制。基础医学院博士研究生李娜、宋晓佳和硕士研究生彭雪琪为共同第一作者,山东大学为第一作者和通讯作者单位。
MASLD-HCC是全球增速最快的肝癌亚型,对现有免疫治疗策略表现出显著抵抗,且目前临床上尚缺乏有效的干预靶点,已成为当前肝癌诊疗领域亟待突破的重大临床难题。脂代谢异常驱动的免疫微环境重塑被认为是该疾病进展的关键因素,但其具体机制尚不明确。亟须深入解析其免疫调控机理,以发现新的治疗靶点。
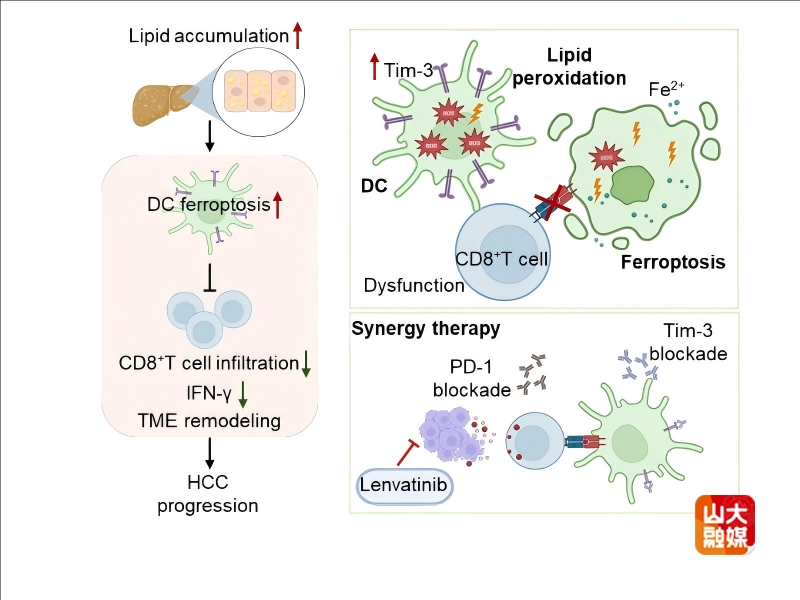
本研究结合单细胞测序、多种MASLD-HCC动物模型及临床样本,系统解析了高脂微环境中树突状细胞(DC)的功能异常及其调控机制。研究发现,MASLD-HCC患者肿瘤组织中DC浸润显著减少,DC与CD8⁺ T细胞之间的互作严重受损,且DC数量的减少与患者不良预后密切相关。机制研究表明,高脂微环境可上调DC表面Tim-3的表达,增强其对游离脂肪酸的摄取,引发脂质积累及过氧化,从而诱导DC发生铁死亡,导致DC耗竭及其抗原提呈功能障碍,最终抑制CD8⁺ T细胞介导的抗肿瘤免疫应答。尤为值得关注的是,Tim-3基因敲除或抗体阻断可有效保护DC免于铁死亡,恢复其免疫激活功能,并与抗PD-1抗体或一线靶向药物仑伐替尼产生协同作用,显著抑制MASLD-HCC进展。该研究不仅阐明了Tim-3在MASLD-HCC免疫逃逸中的关键作用,也为开发靶向Tim-3/铁死亡通路的新型联合治疗策略提供了重要的理论依据和潜在干预靶点。
山东第一医科大学教授唐华为本课题提供了重要帮助和关键材料支持。山东大学基础医学院教授梁晓红、高立芬,副教授武专昌为该研究做出了重要贡献。本研究得到国家自然科学基金、山东省自然科学基金及山东省基础研究特区计划等项目的资助,并得到山东大学转化医学共享平台和基础医学院科研共享平台的大力支持。
马春红教授团队长期致力于肝脏免疫微环境调控和干预策略研究,系统探索HBV、代谢等环境因素诱发肝脏炎症及其恶性转化机制,为肿瘤免疫治疗提供了潜在靶点和新思路。相关成果发表在Sci Immunol、Sci Transl Med、J Hepatol、Nat Commun、J Exp Med、Gastroenterology、Gut、Hepatology、Cancer Res等国际学术期刊。