
[本站讯]近日,山东大学齐鲁医院超声科李杰教授团队在国际学术期刊Journal of Nanobiotechnolog(中科院1区TOP,IF=12.6)发表题为“Ultrasound and ROS-responsive nanodroplets inhibit TCA cycle in hepatocellular carcinoma”的研究论文,该研究构建并验证了一种具有活性氧(ROS)与超声(US)双重响应特性的靶向纳米液滴sGTND,证实sGTND 联合超声靶向微泡破坏(UTMD)技术可通过激活NRF2通路并沉默G6PD表达,协同抑制肝癌细胞三羧酸循环,进而发挥高效抗肿瘤作用。医院硕士研究生赵婷、超声科副主任医师郭鲁、博士研究生丛宁为该论文的共同第一作者,李杰教授为该论文的通讯作者,山东大学齐鲁医院为该论文的第一作者和通讯作者单位。
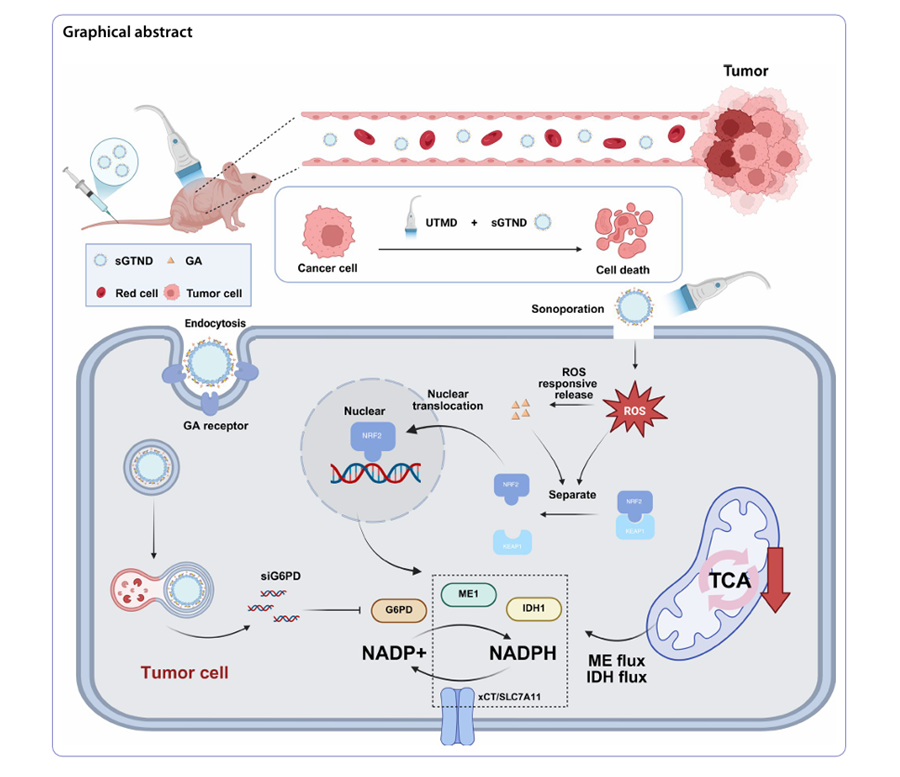
异常能量代谢是肝细胞肝癌(HCC)等多种肿瘤细胞的典型特征。HCC可通过代谢重编程上调三羧酸循环(TCA)与线粒体呼吸以满足其旺盛的能量需求。基于HCC这一核心代谢特征,本研究构建了一种活性氧(ROS)与超声(US)双重响应型纳米液滴,命名为sGTND。首先,通过ROS响应性硫醇键(TK键)将甘草次酸(GA)与羧甲基壳聚糖(CMC)共价偶联,设计并合成新型GTC聚合物;随后以GTC聚合物为壳层、全氟己烷(PFH)为内核,包载葡萄糖-6-磷酸脱氢酶(G6PD)siRNA,最终制备得到sGTND。表征结果显示,sGTND平均粒径为301.7±22.11nm,具备良好的生物相容性及优异的超声增强造影性能。借助GA对肝癌细胞的靶向识别作用,sGTND可特异性靶向并富集于HCC病灶。在超声靶向微泡破坏(UTMD)作用下,原位产生的ROS可断裂TK键并释放GA,进而激活核因子红系2相关因子2(NRF2);同时,UTMD介导的空化效应可触发siRNA释放,实现对G6PD的有效沉默。上述双重作用协同抑制三羧酸循环,最终实现高达95.1%的抗肿瘤效率,显著抑制HCC增殖与转移。此外,sGTND可作为超声造影剂用于增强超声成像(CEUI),实现对肿瘤的精准诊断。综上,sGTND联合UTMD策略通过同步激活NRF2与抑制G6PD,高效阻断TCA循环,为肝细胞肝癌的诊疗一体化提供了一种全新思路。
李杰教授团队长期致力于构建精准医疗下靶向性纳米超声造影剂的肿瘤诊疗一体化系统,对纳米级超声造影剂的优化制备、可视化精准诊疗、肿瘤部位的超声造影成像等进行了深入的基础和临床研究。近年来,课题组在肿瘤精准分子影像、肿瘤可视化治疗及疗效评估方面取得了一系列高水平成果,先后发表于Advanced Science、Biomaterials、Journal of Controlled Release、Journal of Nanobiotechnology等学术期刊,授权相关国家发明专利近10项,研究成果多次在国内外超声医学大会上报告,产生了广泛影响。该研究工作得到了国家自然科学基金、山东省泰山学者计划等项目的资助。