[本站讯]近日,基础医学院赵伟教授团队在《美国国家科学院院刊》(PNAS)发表题为“SCD1 licenses STING signaling through fatty acid desaturation–mediated membrane remodeling”(SCD1通过脂肪酸去饱和介导的膜重塑驱动STING信号通路)的研究论文。该研究发现,代谢酶SCD1可通过调控内质网膜的脂质组成与物理特性,决定固有免疫核心蛋白STING的激活状态,从而精密调控抗病毒免疫反应。基础医学院博士后秦丹慧为第一作者,赵伟教授为通讯作者。山东大学为第一作者和通讯作者单位。
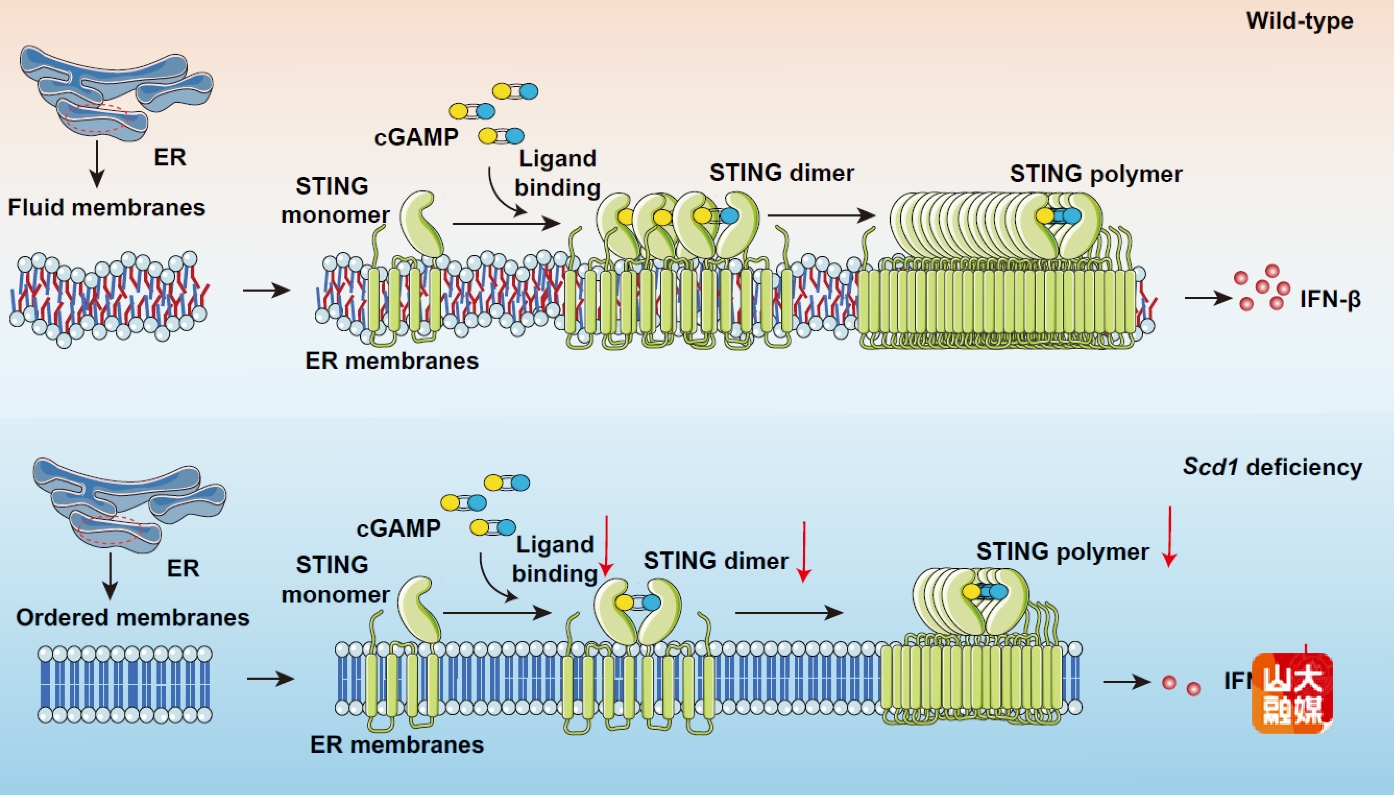
cGAS-STING通路是细胞感知胞质DNA并启动I型干扰素等固有免疫应答的核心,在抗感染及自身免疫疾病中均发挥关键作用。STING作为定位于内质网的适配蛋白,其激活后从内质网向高尔基体的转运是信号启动的关键步骤,该过程受到多种翻译后修饰及细胞微环境的精密调控。然而,细胞代谢状态,特别是脂质代谢如何通过物理性改变膜环境来调控STING功能,此前尚不清晰。硬脂酰辅酶A去饱和酶1(SCD1)是催化饱和脂肪酸(如棕榈酸C16:0、硬脂酸C18:0)转化为单不饱和脂肪酸(如棕榈油酸C16:1、油酸C18:1)的关键代谢酶。该研究发现,SCD1及其产生的单不饱和脂肪酸对DNA病毒(如单纯疱疹病毒HSV-1)触发的STING信号激活至关重要。机制上,SCD1催化生成的单不饱和脂肪酸被特异性整合到内质网膜的磷脂中,改变了膜的脂质组成。这种“脂质重塑”降低了膜的脂质堆积密度,增强了膜的流动性和弯曲度,从而形成了一个更有利于STING蛋白与其配体cGAMP结合、并发生二聚化及构象改变的物理微环境。反之,SCD1缺失或抑制剂处理会导致膜环境趋于“僵硬”,显著抑制cGAMP与STING的结合及后续的TBK1-IRF3信号传导,最终削弱I型干扰素的产生。Scd1基因缺失的小鼠,其STING信号应答受损,在应对HSV-1病毒感染时,体内病毒载量更高,炎症损伤更重,死亡率上升。而通过膳食补充油酸(C18:1)提升单不饱和脂肪酸水平,则可以有效逆转Scd1缺失导致的STING信号缺陷与病毒易感性。这为通过代谢干预(如调节膳食脂肪酸)来调控免疫提供了直接依据。
该研究首次揭示了SCD1驱动的脂肪酸去饱和作为一种“生物物理检查点”,通过直接改变细胞膜属性来“许可”STING激活的新范式。这一机制不同于已知的脂质通过共价修饰(如棕榈酰化)或竞争性结合来调节STING的方式,不仅深化了对固有免疫代谢调控的认识,也为治疗STING过度活化相关的自身免疫疾病或功能低下相关的感染性疾病提供了新的潜在靶点(SCD1)和干预策略(膳食脂肪酸调节)。
赵伟教授团队主要从事固有免疫激活及调控机制研究,为病毒性疾病防治、肿瘤治疗等提供理论依据;相关研究成果发表在Nature Immunology、Immunity、Journal of Clinical Investigation、PNAS、Nature Communications等杂志。本研究得到了国家自然科学基金、山东省重大基础研究项目等资助。