[本站讯]近日,化学与化工学院前沿化学研究院李春霞教授团队在金属螯合疗法抑制肿瘤转移方面取得一系列新进展,在国际期刊Angewandte Chemie International Edition杂志发表了题为“EDTA-Mg Nano-Chelators Amplify Ferroptosis by Artificially Simulating the Epithelial-MesenchymalTransition Process and Endogenous Iron Deprivation”的研究性论文,并被该期刊选为“Hot Paper”。李春霞教授和齐鲁医院(青岛)教授高海东为共同通讯作者,2022级博士研究生解玉林和齐鲁医院(青岛)姜腾飞为共同第一作者。另外,在国际期刊Advanced Materials杂志发表了题为“Antagonistic Iron Competition Induced by Iron Chelators Heightens Cuproptosis in Both Tumors and Intratumoral Bacteria”的研究性论文。李春霞教授为唯一通讯作者,2022级博士研究生解玉林为第一作者。
李春霞教授团队近年来一直探索增强抗肿瘤免疫治疗以及抑制肿瘤转移的研究,近期取得一系列新的进展。传统螯合疗法因缺乏特异性与靶向性,常需严格控制剂量并持续监测患者体征。为了克服这一问题,研究团队提出了一种新型的金属螯合疗法(Angew. Chem. Int. Ed. 2025, 64, e202417592),即通过弱螯合能力的金属离子与螯合剂配位,构建可在肿瘤部位蓄积的纳米螯合剂,在耗竭肿瘤生长所必需的金属离子的同时,释放具有细胞毒性的新型金属离子。该纳米工程化策略不仅提升了螯合剂对特定金属离子的选择性,也增强了其在肿瘤部位的长期蓄积能力。基于此,研究团队从肿瘤的上皮-间质转化(EMT)过程和瘤内菌群出发,以金属螯合疗法为核心,进一步设计了两种治疗策略来打破肿瘤的免疫抑制微环境并有效抑制肿瘤转移。
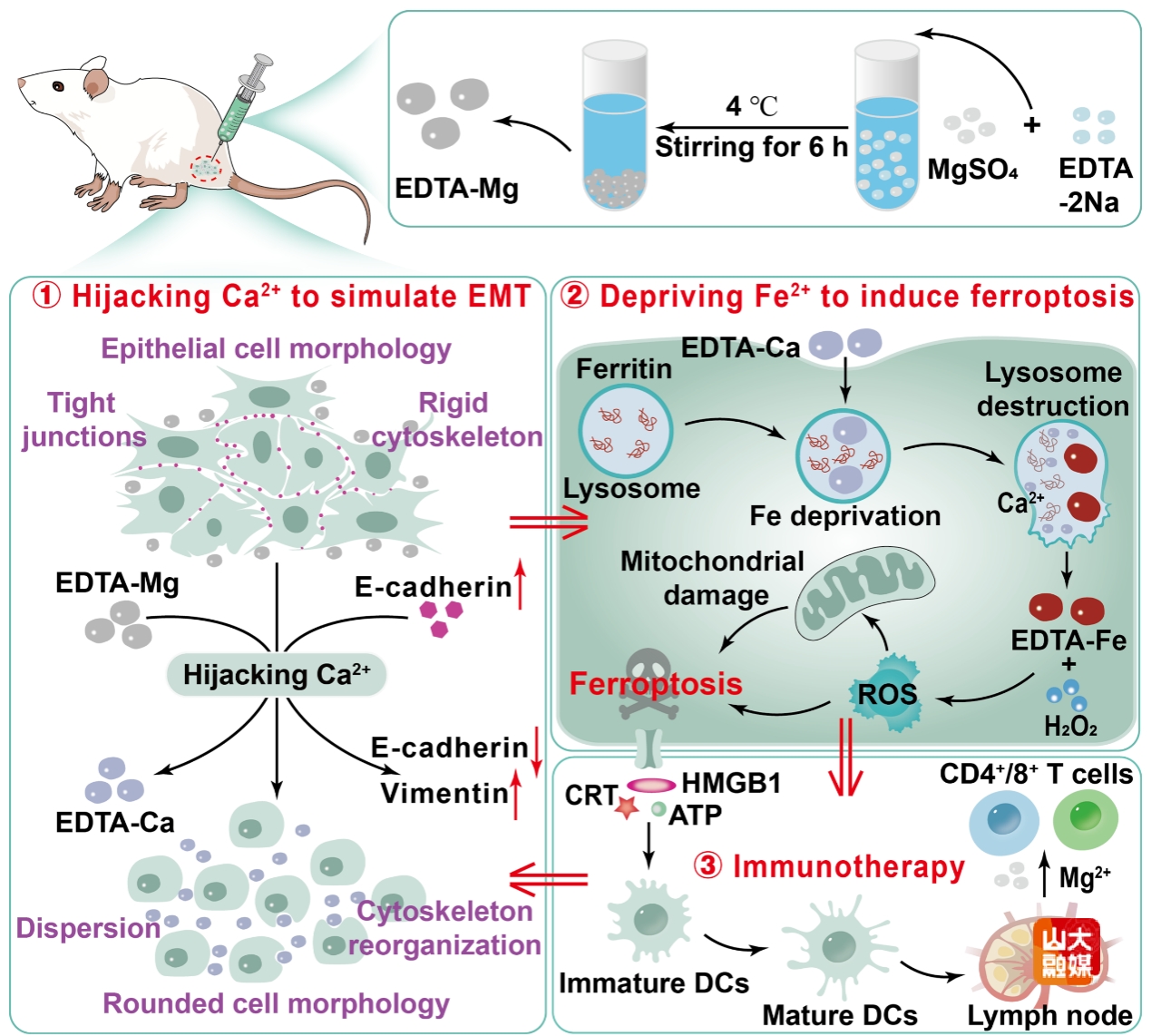
图1. EDTA-Mg的制备及其对肿瘤的抑制机制示意图。
(1)EDTA-Mg纳米螯合剂通过人为模拟EMT过程以及内源性铁剥夺来增强铁死亡治疗。EMT是引发肿瘤转移的关键步骤。通常,研究人员关注的是抑制EMT以防止肿瘤转移。然而,他们忽略了发生EMT的肿瘤细胞更容易受到外界环境的干扰。这一时期的肿瘤细胞是一个潜在的治疗靶点,但精确调控肿瘤细胞的EMT仍然是一个具有挑战性的难点。在此,基于金属螯合疗法,研究团队通过乙二胺四乙酸(EDTA)实现了对肿瘤EMT过程的精准调控和内源性铁剥夺,从而协同增强了肿瘤的铁死亡与免疫治疗效果。具体而言,通过将EDTA与Mg2+配位,制备了一种具有螯合功能的纳米治疗剂(EDTA-Mg)。如图1所示,将EDTA-Mg注射至肿瘤部位后,它首先与肿瘤细胞表面的E-钙黏蛋白相互作用,螯合Ca2+并释放Mg2+,形成EDTA-Ca。此时,由于Ca2+被消耗,肿瘤细胞表面E-钙黏蛋白的表达减少,破坏了肿瘤细胞间的黏附。肿瘤细胞失去极性,细胞骨架发生改变,形态变圆。相应地,肿瘤细胞中波形蛋白和基质金属蛋白酶2(MMP-2)的表达上调。这些变化表明肿瘤细胞中发生了EMT过程。接下来,EDTA-Ca被肿瘤细胞内吞并进入溶酶体。在溶酶体中,EDTA-Ca剥夺铁蛋白中的铁离子并释放Ca2+,从而导致溶酶体破裂并释放出EDTA-Fe。EDTA-Fe与肿瘤细胞中大量存在的H2O2发生芬顿反应,生成大量活性氧(ROS),造成损伤线粒体功能并诱导肿瘤细胞发生脂质过氧化,最终引发铁死亡。死亡的肿瘤细胞释放损伤相关分子模式,促进树突状细胞成熟,并激活抗肿瘤免疫反应。最初释放的Mg2+进一步增强效应T细胞的功能,有效抑制了肿瘤的生长和转移。这种基于EDTA的螯合特性模拟EMT的策略,为肿瘤治疗提供了全新的视角(Angew. Chem. Int. Ed. 2025, 64, e202506126, Hot Paper)。
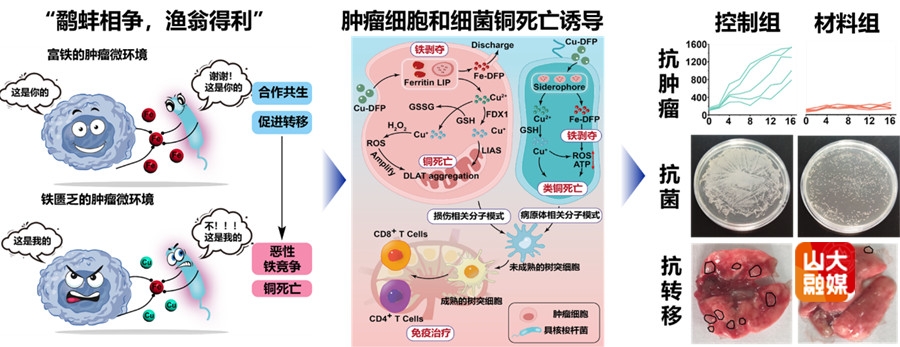
图2. Cu-DFP通过铁剥夺和铜死亡协同抗肿瘤和抗菌作用示意图。
(2)铁螯合剂通过诱导肿瘤和瘤内细菌的对抗性铁竞争来增强铜死亡对两者的治疗效果。铁是维持机体发育的重要微量元素之一,不仅参与氧气运输、电子转移和能量代谢等基本代谢途径,而且在基因表达调控、细胞增殖分化、免疫防御过程中发挥重要作用。由于快速增殖的代谢需求,肿瘤和肿瘤内细菌都表现出铁依赖性,称为“铁成瘾”。受中国寓言“鹬蚌相争,渔翁得利”的启发,研究团队开发了一种铁纳米螯合剂:铜-去铁酮(Cu-DFP),该纳米螯合剂能够在肿瘤微环境中耗竭铁元素并释放铜离子,从而在肿瘤细胞和瘤内细菌中同时诱导双重的铜死亡。如图2所示,富含铁元素的肿瘤微环境通常维持着肿瘤细胞与瘤内细菌的代谢共生状态。这些细菌不仅促进肿瘤进展,还会营造免疫抑制微环境。Cu-DFP治疗通过耗竭铁离子来打破这种平衡,将二者的关系转变为对稀缺铁资源的致命竞争,恰如寓言中陷入相互毁灭性争斗的鹬(肿瘤细胞)与蚌(细菌),而治疗策略(“渔翁”)则从中获得治疗优势。研究结果表明,Cu-DFP通过耗竭铁和诱导铜过载实现对肿瘤细胞和瘤内细菌的双重攻击。在肿瘤细胞中,Cu-DFP通过耗竭不稳定铁池并抑制铁蛋白表达来破坏铁稳态,同时释放的Cu2+通过耗竭谷胱甘肽(GSH)和诱导二氢硫辛酰胺S-乙酰转移酶(DLAT)聚集来引发铜死亡。与此同时,缺铁的细菌会增加铁载体的产生,但也会遭受铜介导的氧化应激和能量崩溃。由此引发的细胞死亡会释放具有免疫刺激作用的损伤相关分子模式和病原体相关分子模式,从而促进树突状细胞成熟,有效将免疫抑制的肿瘤微环境转化为免疫激活状态。Cu-DFP介导的金属螯合治疗实现了抗肿瘤,抗菌和抗转移的协同治疗效果。这种利用肿瘤与其定植菌群之间代谢竞争的创新策略,代表了面向微生物群的肿瘤疗法中一项颇具前景的突破(Adv. Mater.2026, 38, e15904)。
上述研究成果拓展了抑制肿瘤转移的治疗策略,为深入了解肿瘤转移过程打下坚实的基础。此外,李春霞教授团队提出的金属螯合疗法不仅适用于乳腺癌,而且其对于其它类型的癌症治疗也具有潜在的应用价值。上述工作得到了国家自然科学基金原创探索延续资助项目、面上项目、青岛市科技惠民项目等多个项目资助。