[本站讯]近日,山东大学基础医学院高成江教授团队在Proc. Natl. Acad. Sci. U.S.A.(美国科学院院刊)(中科院一区TOP期刊,五年IF:10.6)发表了题为"The Crohn's disease–related RNF123 prevents NLRP3 inflammasome assembly by catalyzing unanchored K63-linked ubiquitination on NEK7 "的研究论文。基础医学院免疫学系副研究员刘峰和博士后庄万欣为共同第一作者,刘峰和高成江教授为共同通讯作者。山东大学为第一作者和通讯作者单位。
炎症小体是固有免疫系统的重要组成部分,是介导炎症反应的核心。机体受到病原体感染时,炎症小体激活可以诱发抗感染免疫反应,但是炎症小体的异常激活也会导致机体炎症损伤,构成众多炎症性疾病的发病基础。因此,调控炎症小体激活,维持炎症反应稳态,具有重要意义。
基于GWAS提示的与炎症性肠病相关SNP分析,高成江教授团队首先对克罗恩病相关SNP RNF123-R854H(rs34823813)开展研究。利用Rnf123-R854H突变和Rnf123基因敲除小鼠,研究团队发现在DSS诱导肠炎模型中,该Rnf123突变或Rnf123基因缺失会加重小鼠肠道炎症,且该作用依赖于NLRP3。另外,研究团队发现敲除Rnf123基因也会加重LPS诱导的脓毒血症和Aluminum诱导的腹膜炎。同时,敲除Rnf123基因会通过NLRP3依赖途径增强宿主对细菌感染的抵抗能力。在巨噬细胞中,敲除Rnf123基因或Rnf123基因R854H突变会增强NLRP3炎症小体激活。以上研究证明,RNF123能够特异性调控NLRP3炎症小体激活。进一步,研究团队发现RNF123能够催化NEK7的非锚定K63多聚泛素化修饰,该修饰在NEK7与NLRP3的结合区域形成空间位阻,阻止NEK7解聚NLRP3抑制性“笼状”聚集体,进一步阻碍炎症小体蛋白复合体组装。RNF123的R854H突变导致RNF123对NEK7的催化活性降低,减弱了其对炎症小体激活的抑制作用。最后,研究团队利用纯化蛋白构建了炎症小体体外反应体系,利用体外生化实验,研究团队发现NEK7在体外体系可以直接捕获非锚定K63多聚泛素链,抑制NEK7对NLRP3聚集体的解聚作用和后续的蛋白复合体组装。
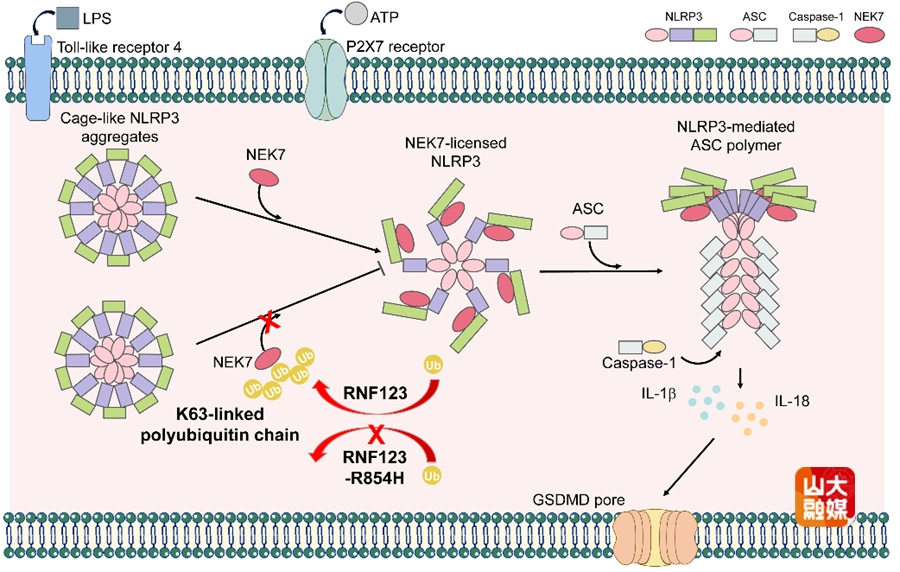
RNF123通过催化NEK7非锚定K63多聚泛素化调控NLRP3炎症小体激活(Liu F et al. PNAS.2026)
本研究阐明了RNF123的SNP突变通过影响NLRP3炎症小体激活加剧肠道炎症的分子机制,构建了“易感基因变异—炎症小体关键蛋白泛素化修饰改变—NLRP3炎症小体过度激活—肠道炎症表型”的完整调控轴,为炎症性肠病的致病机制提供新的见解。同时,本研究揭示了RNF123作为NLRP3炎症小体的关键内源性“分子刹车”和维持炎症反应稳态的重要“调控者”的新角色,提出了非锚定泛素化修饰这一炎症小体新的翻译后修饰类型和调控机制,拓展了对炎症小体激活和炎症反应稳态调控的认知。
高成江教授团队长期致力于固有免疫识别与活化的调控机制研究,近年来在Nature Immunology、Immunity、Journal of Experimental Medicine、PNAS、Cellular Molecular Immunology、Nature Communications、Science Advances等权威杂志上发表了多项研究成果。本研究得到了国家自然科学基金、国家重点研发计划以及山东省自然科学基金等的资助。