[本站讯]近日,山东大学数学与交叉科学研究中心、教育部非线性期望前沿科学中心杨建益教授团队在生物学权威期刊Nature Biotechnology(IF:41.7)发表题为“Integrated experimental and AI innovations for RNA structure determination”的观点(Perspective)文章。该文章系统性回顾了RNA结构测定领域的最新革命性进展,深刻剖析了实验技术与人工智能(AI)从“并行发展”走向“深度融合”的变革趋势,并为解析RNA世界的复杂性提供了前瞻性的路线图。数学与交叉科学研究中心博士后王文恺、博士研究生苏宝泉为论文共同第一作者,杨建益教授、彭珍玲教授为共同通讯作者,山东大学数学与交叉科学研究中心为唯一完成单位。

RNA作为细胞内关键的“社交”介质,其功能的发挥依赖于复杂的三维结构。然而,受限于RNA高度的动态性和独特的理化性质,其结构解析长期面临巨大挑战。近年来,随着冷冻电镜(Cryo-EM)分辨率的突破和以trRosettaRNA为代表的AI预测算法的发展,该领域迎来了新的机遇。杨建益教授团队长期深耕于生物大分子结构预测领域,基于深厚的学术积累,在文中对这一快速发展的交叉前沿领域进行了全景式扫描及展望。
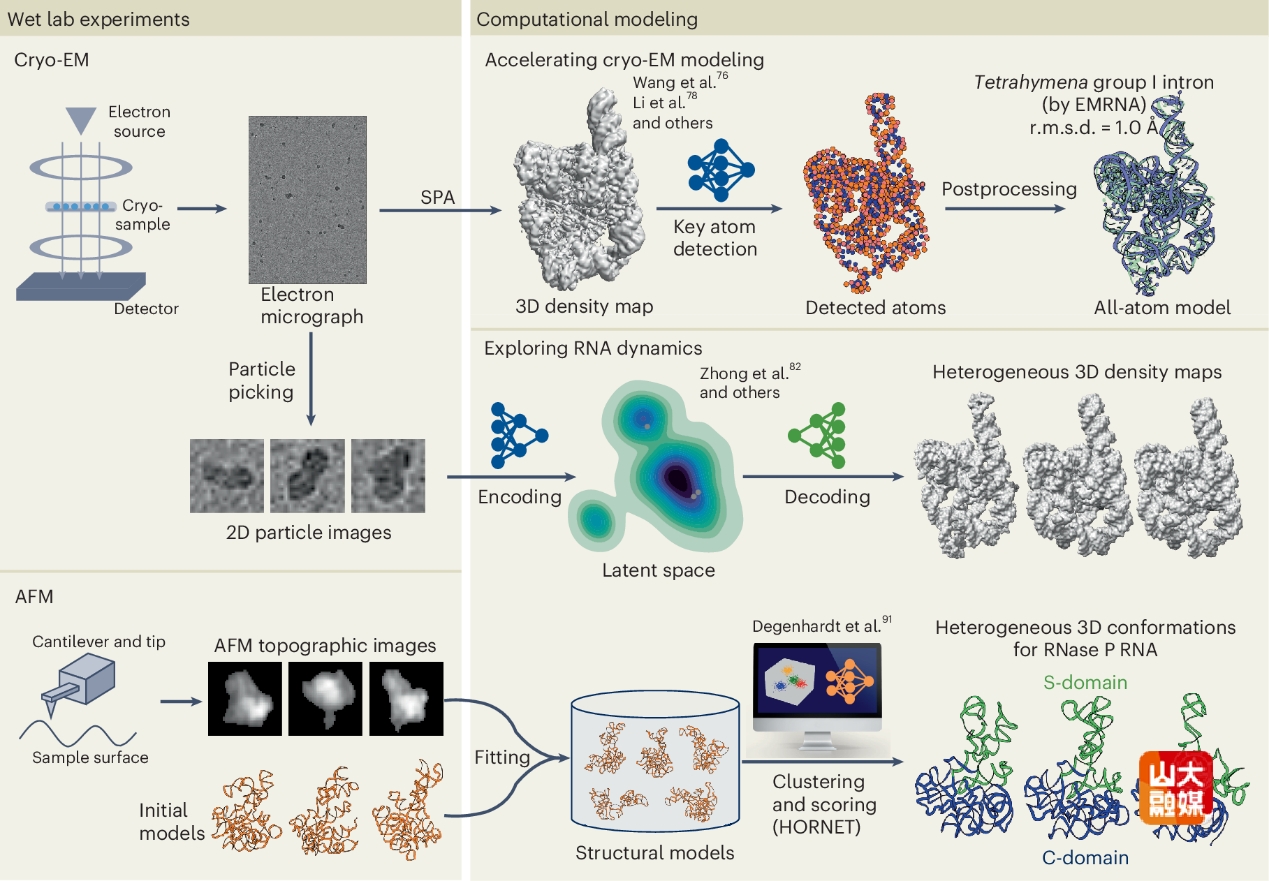
文章指出,传统的实验方法与计算预测曾是独立发展的平行线,而现在正通过互补整合迈向新的阶段。在实验维度,文章主要分析了基于RNA“支架(scaffold)”策略和下一代电子探测器等技术如何突破Cryo-EM的分辨率限制;在计算维度,文章梳理了AI预测模型从分步式(two-step)到端到端(end-to-end)的演变历程,特别指出了受AlphaFold启发的深度学习架构在RNA领域的巨大应用潜力。
文章的核心观点在于,实验与计算的深度融合已成为推动该领域发展的核心驱动力。文中重点阐述了这一融合趋势下的创新实践:例如,利用EMRNA等深度学习工具,实现了从冷冻电镜密度图到全原子结构的快速自动化建模,效率与精度均显著优于传统方法;同时,通过HORNET等计算框架,结合原子力显微镜(AFM)的低分辨率形貌数据,成功解析了RNA复杂的动态构象系综。
基于上述分析,文章提出了未来该领域的三大关键方向:一是发现新型结构化RNA以丰富数据资源;二是利用AI技术加速结构测定流程;三是开发能够整合多种模态实验数据的新一代AI生成模型。这项工作不仅为理解RNA世界的复杂性提供了清晰的指引,也标志着结构生物学正在全面进入实验与计算协同驱动的新时代。
杨建益教授团队长期致力于生物大分子结构预测算法研究,开发了trRosetta、trRosettaRNA、CryoAtom等多个具有国际影响力的算法工具。在CASP国际蛋白质结构预测竞赛中,团队在蛋白质及RNA结构预测赛道均取得自动算法组冠军。相关研究成果已发表于Nature Methods、Nature Structural & Molecular Biology、PNAS等顶级期刊。
本项研究工作得到国家重点研发计划、国家自然基金委青A、青B及重点项目等基金的资助。