[本站讯]近日,山东大学微生物改造技术全国重点实验室祁庆生/侯进团队在Chemical Engineering Journal期刊上发表了题为“Rewiring energy homeostasis inYarrowia lipolyticaenables efficient terpenoid biosynthesis”的研究成果。该研究通过全局代谢重塑,将碳流从“代谢溢流”转向高效合成β-法尼烯,最终实现82.1 g/L的产量,创下解脂耶氏酵母中萜类化合物的最高生产纪录。山东大学微生物改造技术全国重点实验室博士后刘晓芹为第一作者,祁庆生教授和侯进教授为通讯作者,山东大学微生物改造技术全国重点实验室为第一完成单位和通讯作者单位,清华大学李斐然老师为该工作提供了重要帮助。

“溢流代谢”与“碳通量竞争”一直是制约微生物细胞工厂生物制造效率的重要评价。解脂耶氏酵母是萜类化合物的优良底盘,但其天然的柠檬酸溢流和脂质合成严重分散了碳源,限制了生物合成效率。β-法尼烯是一种无环倍半萜,是合成维生素E的关键中间体,其加氢衍生物法尼烷因其优异的燃烧效率和环境友好特性,成为一种前景广阔的生物燃料候选物。
该研究通过在解脂耶氏酵母中引入非氧化糖酵解(NOG)途径并阻断核心糖酵解,构建了一株用于生产β-法尼烯的非氧化糖酵解酵母。然而,阻断糖酵解途径引发了菌株的生长缺陷。通过适应性实验室进化,结合多组学与通量平衡分析发现:碳阻遏调控因子Reg1与葡萄糖激酶Glk1的同时失活,可通过激活Snf1激酶介导的碳信号通路,协调非氧化糖酵解途径与TCA循环之间的通量,从而重建细胞能量稳态。这导致细胞合成代谢被抑制,而分解代谢被激活。通过代谢工程强化甲羟戊酸途径,促使更多的碳源流入了β-法尼烯的合成,同时副产物合成大幅度降低。
该研究揭示了Snf1激酶在全局代谢重布线中的核心作用,通过双碳源发酵,最终实现了82.1 g/L 的β-法尼烯的高产,转化率为0.21 g/g底物。柠檬酸溢流被完全消除,甘露醇等副产物积累极低。这不仅刷新了该菌株生产萜类化学品的纪录,更证明了通过“能量稳态重构”解决细胞代谢刚性的巨大潜力,为萜类化合物的高效生物合成提供了重要参考。
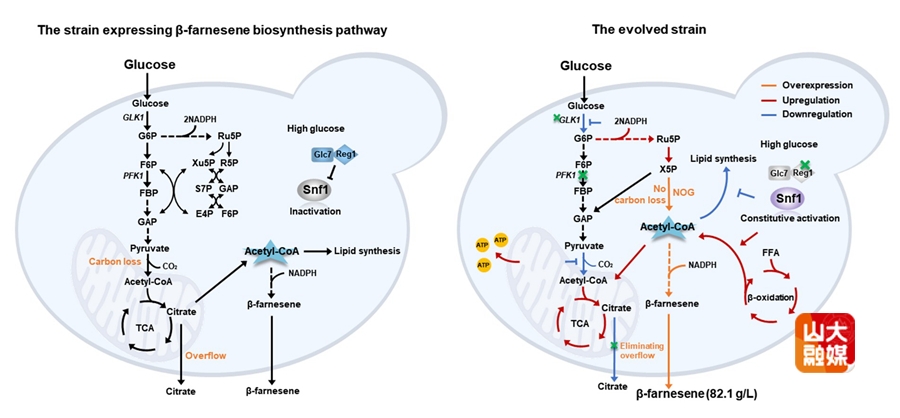
与仅表达β-法尼烯生物合成途径的参考菌株相比,进化菌株的代谢变化
研究得到国家重点研发计划、国家自然科学基金、山东省自然科学基金、泰山学者计划等项目的资助。