[本站讯]近日,山东大学齐鲁医院心内科和络病理论创新转化全国重点实验室郝盼盼教授、卜培莉教授、张梅教授研究团队在心血管疾病的基础研究中取得了一系列重要进展,相关研究发表在Advanced Science(中科院1区Top,5年IF = 15.6)、Theranostics (中科院1区Top,5年IF = 13.1)、Research(中科院1区Top,5年IF = 10.3)和Arteriosclerosis, Thrombosis and Vascular Biology(中科院1区Top,IF = 8.6),受到国内外学术界的高度关注。
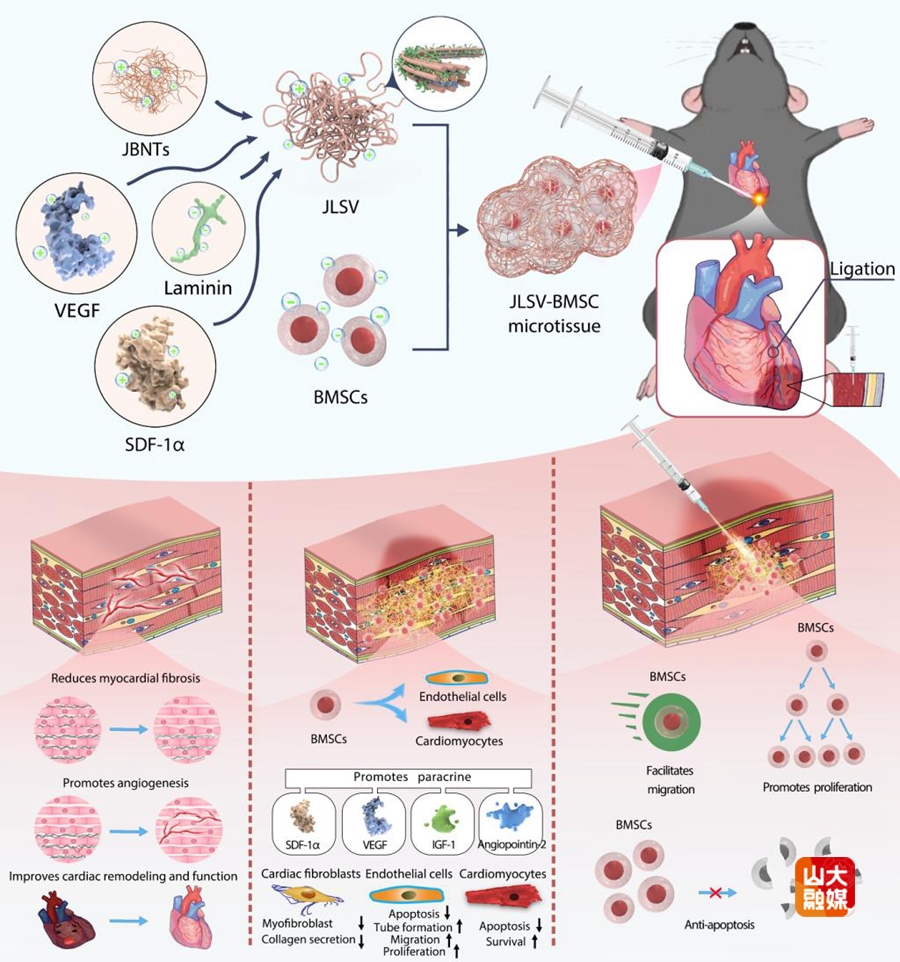
急性心肌梗死具有高发病率和高死亡率,已成为全球的重大公共卫生问题。尽管现代化的血运重建和药物治疗可快速恢复心肌灌注并降低患者住院期死亡风险,但仍无法挽救已经坏死的心肌细胞。心肌细胞一旦坏死便无法自主再生,进而导致进行性心脏重构和心力衰竭。近年研究发现,骨髓间充质干细胞(BMSC)在体外可分化为心肌样细胞,为心肌细胞再生提供了新的希望。然而心肌梗死后,心肌细胞丢失、炎症反应和细胞外基质降解可改变心肌微环境,形成一个严重限制BMSC存活、迁移和分化的恶劣微环境。为了解决这一瓶颈问题,齐鲁医院络病理论创新转化全国重点实验室郝盼盼教授和山东大学药学院周丽波副研究员研究团队跨学科合作,成功开发出一种新型可注射仿生微组织系统,该系统包含由Janus基础纳米管、层粘连蛋白、基质细胞衍生因子- 1α和血管内皮生长因子(JLSV)组成的双仿生细胞外基质支架,用于递送BMSCs(JLSV-BMSC微组织)。其中,JBNTs在结构上模拟了天然心肌ECM的螺旋纳米拓扑形态,为细胞黏附和生长提供力学支持,而SDF-1α、VEGF和层粘连蛋白等生物活性因子具有协同作用,可共同调控干细胞的存活、增殖、定向分化以及血管生成过程。体外实验表明,在氧和糖剥夺条件下,该微组织增强了BMSCs的存活、增殖、迁移、抗凋亡能力和旁分泌信号传导。体内研究显示,该微组织显著提高了BMSCs在梗死部位的留存率,引导BMSCs分化为心肌细胞和内皮细胞,减少了心肌纤维化和细胞凋亡,并促进了血管生成,有助于改善心脏重构和功能。这些结果表明,JLSV - BMSC微组织是一种有前景的心肌梗死治疗策略,可解决基于干细胞疗法的关键难题。该研究发表于国际权威期刊Advanced Science,齐鲁医院心内科硕士生姚丽娜为该文的第一作者,郝盼盼教授、周丽波副研究员为该文共同通讯作者,山东大学齐鲁医院为该文的第一和通讯作者单位。
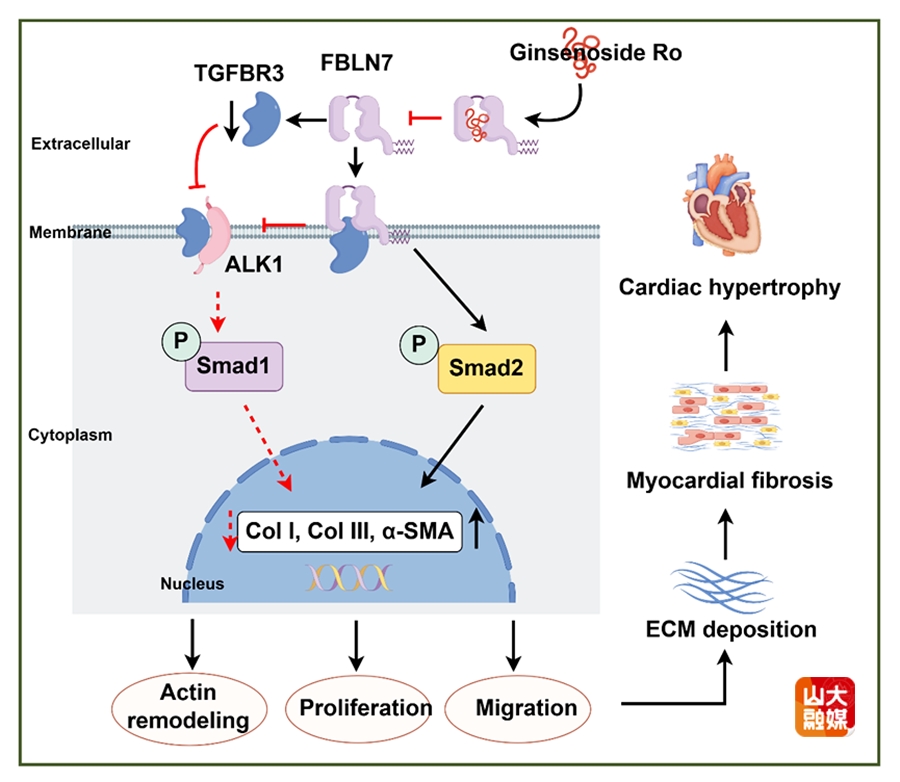
衰老是心血管疾病的重要危险因素,心肌纤维化是衰老相关心脏疾病的特征。近期研究发现,基质细胞蛋白促进细胞衰老和胶原沉积的相互作用,可能成为干预衰老相关心肌纤维化中的重要靶点。已知细胞外基质蛋白Fibulin 7(FBLN7)在肾小管钙化、肿瘤转移、血管新生等病理生理过程中发挥重要作用,但FBLN7与年龄相关心肌纤维化的关系尚不明了。齐鲁医院络病理论创新转化全国重点实验室卜培莉教授研究团队首先在野生型的自然衰老和年轻对照小鼠中检测了FBLN7的表达水平,发现FBLN7在衰老小鼠的心肌组织和血清中表达明显增多。继之,该团队在自然衰老小鼠中构建了FBLN7敲除模型,发现FBLN7敲除显著改善了衰老小鼠的心肌纤维化和心脏舒张功能。整合单细胞测序、蛋白组学测序及荧光共定位分析的结果显示,与正常成纤维细胞相比,衰老成纤维细胞表现出胶原合成等促纤维化能力下降,敲低FBLN7可促进这一现象,从而抑制衰老心脏的心肌纤维化。反之,在心脏成纤维细胞中过表达FBLN7可加剧衰老小鼠的心功能异常和心肌纤维化。体外实验证实,衰老成纤维细胞表现出胶原合成等促纤维化能力下降,过表达FBLN7可抑制这一现象。机制研究显示,FBLN7可调控TGF-βs信号转导,至少部分通过抑制ALK1-Smad1/5/9信号通路发挥作用。分子对接、免疫共沉淀等实验发现,FBLN7结合TGFBR3并下调其表达,而过表达TGFBR3可逆转FBLN7对ALK1-Smad1/5/9通路的抑制并激活Smad2信号,证明了TGFBR3在FBLN7介导的TGF-βs信号转导中的关键作用。最后,研究团队通过虚拟筛选、分子动力学模拟和表面等离子共振(SPR)等技术筛选出与FBLN7存在物理相互作用的天然产物-人参皂苷Ro(GRO),并在体内和体外实验中证明,GRO抑制FBLN7过表达所致的衰老成纤维细胞的胶原合成增加,改善衰老小鼠的心肌纤维化和心功能异常。该研究不仅揭示了FBLN7在年龄相关心肌纤维化中的核心调控作用,还筛选出具有治疗作用的小分子天然产物,为衰老相关疾病的靶向干预和药物研发提供了依据。该研究发表于国际权威期刊Theranostics,齐鲁医院心内科博士后郑雪慧为该文的第一作者,卜培莉教授为该文的通讯作者,山东大学齐鲁医院为该文的第一和通讯作者单位。
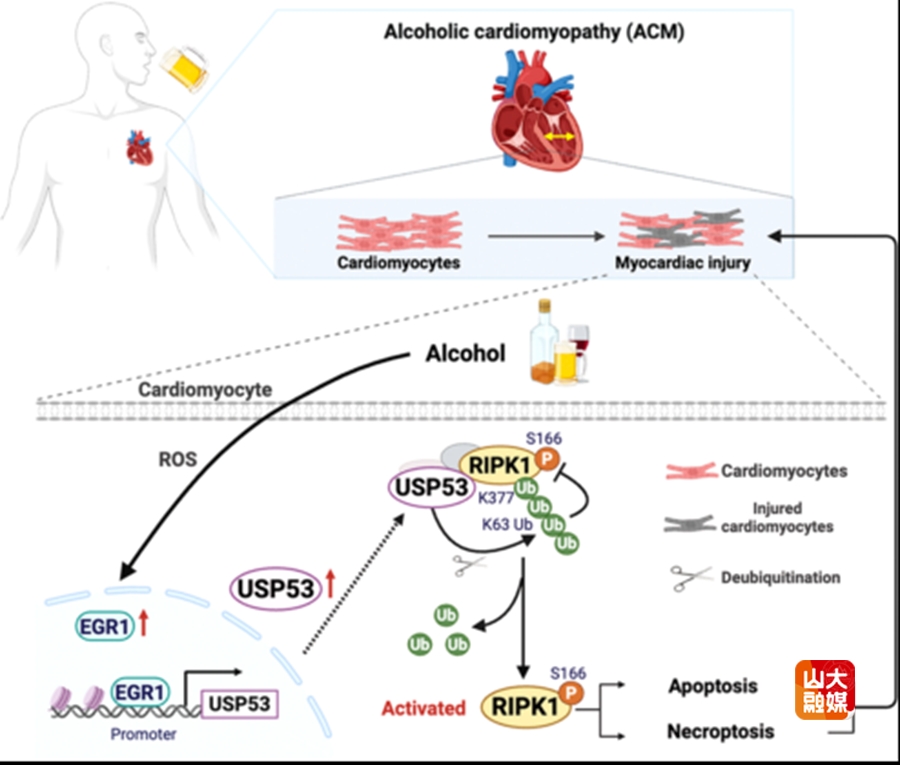
酒精性心肌病(ACM)是由长期过量饮酒引发的扩张型心肌病,其主要病理机制在于酒精诱导的心肌细胞损伤或死亡。以往研究表明,受体相互作用蛋白激酶1(RIPK1)作为控制细胞死亡途径的关键介质,活性受到泛素化、去泛素化和磷酸化等多种翻译后修饰过程的调控,但RIPK1在ACM的发生和发展中的作用不明。泛素特异性蛋白酶53(USP53)在心肌组织中高表达,以往研究发现USP53的活性与细胞死亡调控密切相关,但USP53在ACM发生和发展中的作用和机制亦不明确。针对这些科学问题,齐鲁医院络病理论创新转化全国重点实验室张梅教授团队与山东大学基础医学院戴珅副研究员和刘凤鸣研究员团队合作,建立了体内和体外ACM模型,发现乙醇喂养小鼠出现明显的心室扩大、心脏收缩功能障碍和心肌纤维化程度增加。同时,酒精显著上调了心肌组织和心肌细胞中凋亡标志蛋白cleaved caspase-3和程序性坏死标志蛋白pRIPK3和pMLKL的表达水平。此外,乙醇暴露可促进受体相互作用丝氨酸/苏氨酸蛋白激酶1(RIPK1)自磷酸化,并增强pRIPK1相关的凋亡和坏死性凋亡。通过免疫共沉淀(Co-IP)结合液相色谱-串联质谱(LC-MS/MS)分析,确定泛素特异性蛋白酶53(USP53)是心肌细胞中乙醇刺激后调节RIPK1激活的关键去泛素化酶。机制研究证明,乙醇通过早期生长反应因子1(EGR1)的转录诱导作用上调USP53。随后,USP53与RIPK1的中间结构域相互作用,去除赖氨酸- 377(K377)处的K63相关泛素化,促进RIPK1磷酸化,并触发心肌细胞下游的凋亡和坏死性凋亡途径。此外,与对照组相比,乙醇喂养的心肌细胞特异性USP53敲除(USP53CKO)小鼠生存率提高,心肌细胞死亡减少。上述研究确实了USP53是RIPK1依赖性细胞死亡的新型调节因子,增进了对ACM机制途径的理解,提示USP53 - RIPK1信号轴可作为缓解ACM进展的潜在治疗靶点。该研究发表于国际权威期刊Research,齐鲁医院心内科博士生潘继琛为该文的第一作者,张梅教授、戴珅副研究员、刘凤鸣研究员为该文的共同通讯作者,山东大学齐鲁医院为该文的第一和通讯作者单位。
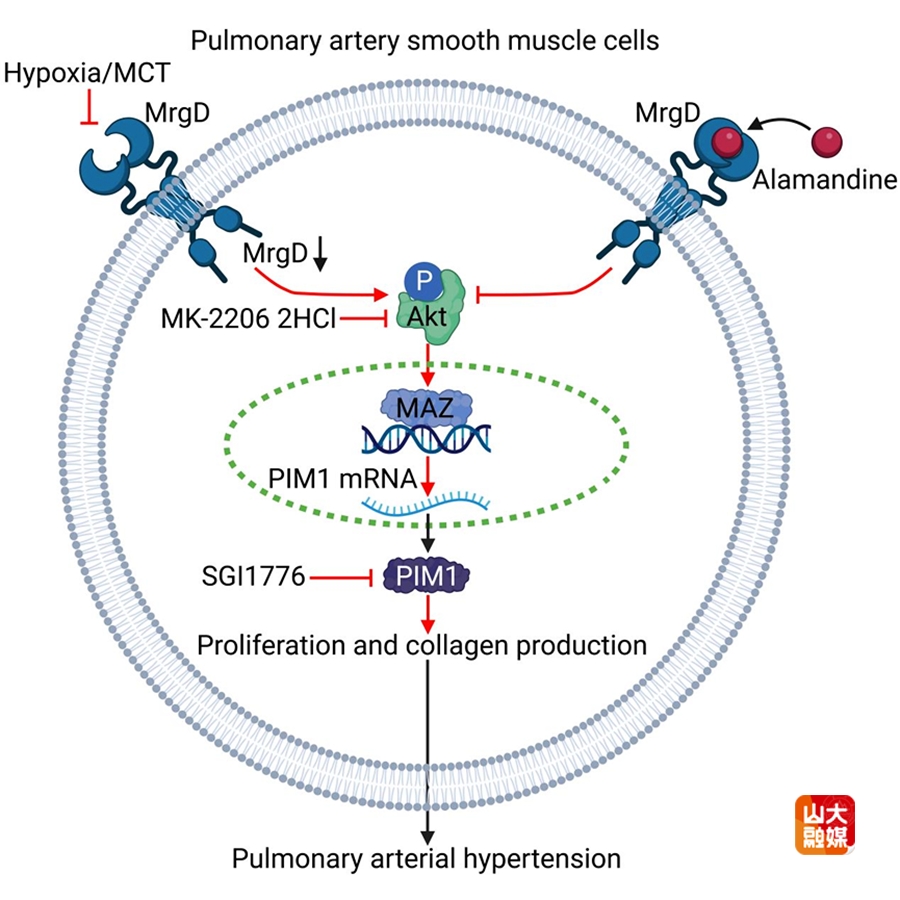
肺动脉高压(PH)是一种进行性发展的心血管疾病,主要病理特征为肺血管系统重构、右心室肥厚和纤维化。由于目前临床上仍缺乏有效逆转肺血管重构的手段,患者生活质量极差,病死率极高。探索肺动脉高压的发病机制和干预靶点,对于靶向药物研发和治疗方案创新具有重要的临床意义。
近年研究发现,Mas相关G蛋白偶联受体成员D(MrgD)在心血管系统中高表达,具有抑制炎症反应、促进血管舒张、改善纤维化等保护作用。然而,MrgD在PH发病中的作用和机制不明。齐鲁医院络病理论创新转化全国重点实验室郝盼盼教授团队在临床和动物样本中发现,肺动脉平滑肌中MrgD的表达水平与PH的进展存在负相关。该团队利用Sugen5416联合低氧刺激构建PH小鼠模型并利用野百合碱刺激构建PH大鼠模型,继之采用MrgD基因全身敲除和血管平滑肌细胞特异性敲除技术,探索了MrgD缺失或激活对PH的影响,发现MrgD缺失通过激活AKT磷酸化,上调转录因子MAZ表达,MAZ直接结合PIM1启动子(-973至-399 bp区域),驱动肺动脉平滑肌细胞增殖与胶原沉积。使用PIM1抑制剂SGI1776或敲低PIM1可恢复MrgD缺失导致的病理表型,证实了MrgD-PIM1轴在PH发病中的核心调控作用。该研究首次揭示了MrgD通过AKT-MAZ-PIM1信号轴调控缺氧性PH的核心机制,为理解PH病理进程提供了新视角,奠定了MrgD作为治疗靶点的理论基础。该研究发表于国际权威期刊Arteriosclerosis, Thrombosis and Vascular Biology,美国心脏协会(AHA)中文官方公众号对本研究进行了专题报道。齐鲁医院心内科博士生钟鸿钰(现就职于福建医科大学附属协和医院心血管内科)为该文的第一作者,郝盼盼教授为该文的通讯作者,山东大学齐鲁医院为该文的第一和通讯作者单位。