[本站讯]近日,山东大学齐鲁医院神经外科倪石磊课题组在中枢神经肿瘤和退行性疾病研究领域取得系列新进展,相关研究成果相继发表于Advanced Materials(中科院1区Top期刊,IF:26.8)、Nature Communications(中科院1区Top期刊,IF:17.2)和Science Advances(中科院1区Top期刊,IF:14.1)等国际期刊,并在Nature(中科院1区Top期刊,IF:55)发表学术观点。
胶质母细胞瘤(GBM)是成人中枢神经系统最常见且恶性程度最高的原发性肿瘤,患者中位生存期通常不超过15个月,五年生存率低于5%。目前,GBM的标准治疗方案为最大安全程度的手术切除联合放疗及口服替莫唑胺,但治疗效果有限,亟需探索新的治疗方式以解决临床治疗困境。
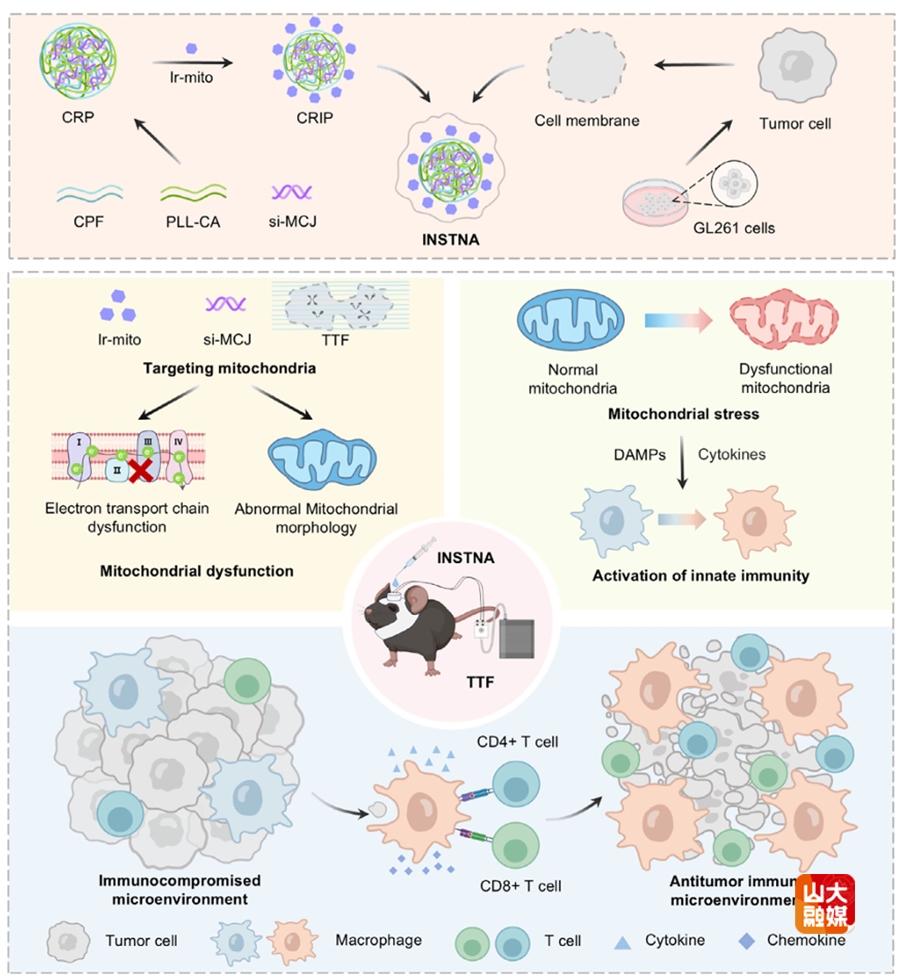
图1 胶质瘤局部INSTNA激活先天免疫示意图
先天免疫在协调脑内免疫反应中发挥关键作用,然而,GBM已演化出逃逸机制以逃避免疫监视,给现有免疫治疗带来了重大挑战。基于此,研究团队开发了一种新型局部免疫治疗策略,旨在通过靶向诱导线粒体应激来重新激活GBM的先天免疫反应,从而增强肿瘤免疫原性。具体而言,研究团队构建了先天免疫激活纳米颗粒(INSTNA),其内包载有带正电的铱基复合物以及针对甲基化控制J蛋白的小干扰RNA,以削弱肿瘤细胞线粒体呼吸。INSTNA可有效破坏GBM细胞的线粒体功能,尤其在联合肿瘤电场治疗时效果更为显著。所设计的电荷翻转型INSTNA可抑制线粒体电子传递链,诱导氧化磷酸化应激,并导致线粒体基质内容物释放。此外,在术后GBM小鼠模型中,基于水凝胶的INSTNA给药方式可显著重塑免疫抑制性肿瘤微环境,从而诱导明显的肿瘤清除。研究结果表明在术后GBM中靶向诱导线粒体应激可增强先天免疫激活并提高适应性免疫应答,为缓解GBM复发提供了一条有前景的治疗途径。该研究成果近日发表于Advanced Materials,齐鲁医院神经外科倪石磊、张玉霖,湖南科技大学李毅为论文共同通讯作者;第一临床学院研究生韩旭、封帆、王梓旭为共同第一作者。
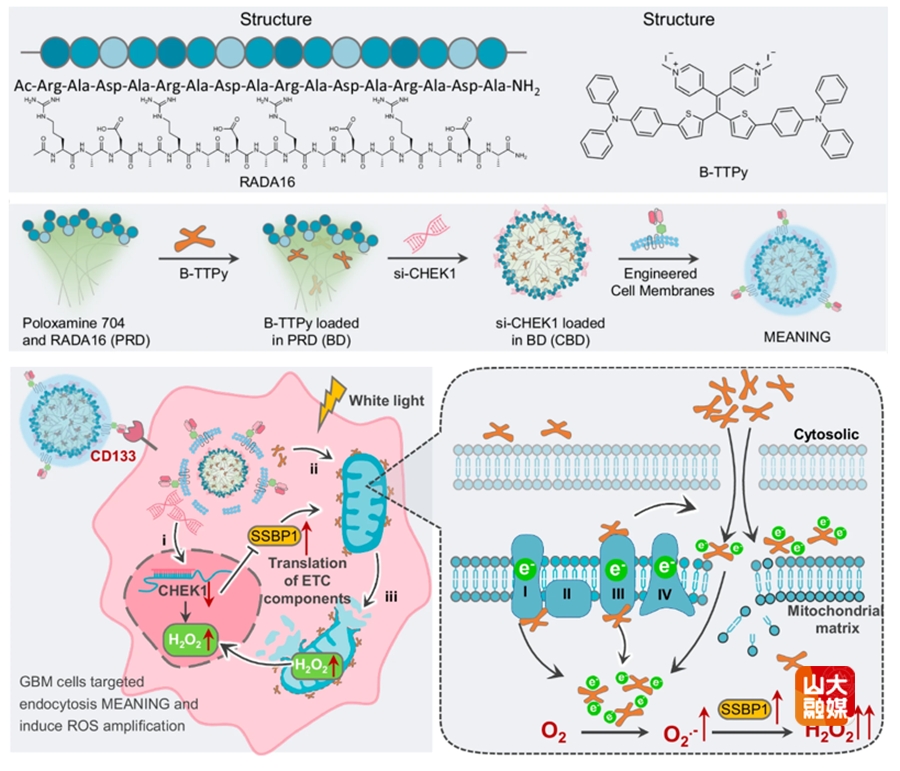
图2 MEANING靶向线粒体ETC治疗示意图
胶质母细胞瘤的低免疫原性和免疫抑制微环境导致现阶段免疫检查点抑制剂治疗效果不佳,T细胞、巨噬细胞等免疫细胞无法识别低免疫原性肿瘤细胞是导致肿瘤术后复发的关键。
为克服GBM免疫原性低的特性,研究团队提出了一种通过原位操控线粒体电子传递链(ETC)激活内源性cGAS-STING信号通路,以增强GBM免疫应答的策略。在白光照射下,合成的蝴蝶状光敏剂B-TTPy通过产生过量活性氧破坏线粒体ETC。协同作用下,抑制检查点激酶 1(CHK1)可进一步加剧ETC功能障碍,从而增强B-TTPy对肿瘤细胞的细胞毒性。研究结果显示,自主开发的线粒体电子调控纳米颗粒(MEANING)可高效激活先天与适应性免疫反应,通过募集抗原递呈细胞和细胞毒性T细胞至术腔边缘,从而增强局部抗肿瘤免疫。此外,结合可降解水凝胶的术腔局部给药可重塑免疫抑制性肿瘤微环境并清除残余GBM细胞。综上所述,本研究开发了一种针对GBM的局部免疫激活策略,以预防术后复发,并揭示了ETC阻断作为低免疫原性肿瘤潜在治疗策略的应用前景。该研究成果近日发表于Nature Communications,齐鲁医院神经外科倪石磊、张玉霖,西北农林科技大学张艳荣为论文共同通讯作者;第一临床学院研究生房泽正、王军鹏,西北农林科技大学研究生程璐璐为共同第一作者。
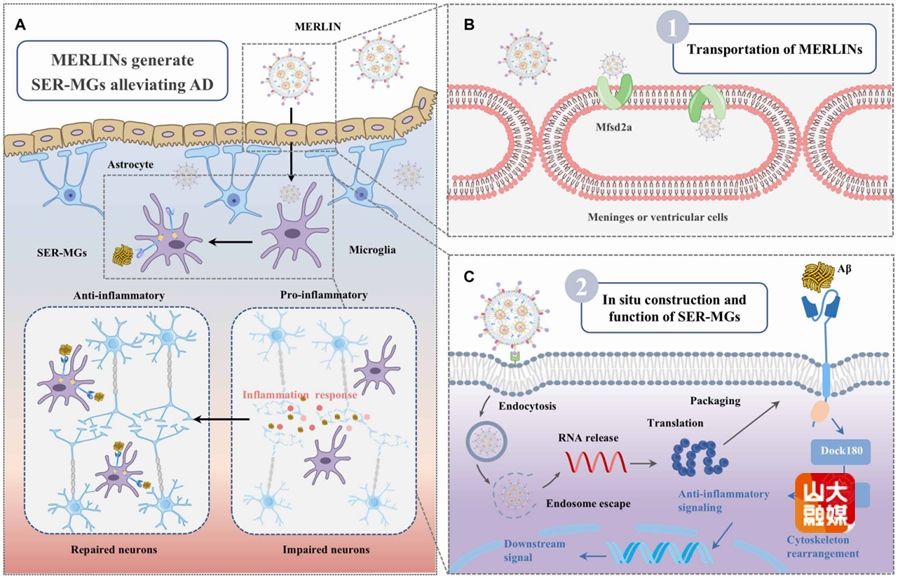
图3 油酸衍生LNP跨生物屏障在体生成工程化小胶质细胞用于AD小鼠淀粉样蛋白非炎性清除示意图
阿尔茨海默病是一种中枢神经系统的慢性神经退行性疾病,随着我国人口老龄化进程的加快,预计到2050年我国60岁以上阿尔茨海默病患者人数可能达到2765万,已成为重要的公共卫生挑战。
靶向清除淀粉样蛋白β(Aβ)的单克隆抗体免疫治疗在阿尔茨海默病研究中备受关注,但其伴随的Fc受体激活及促炎效应可加剧神经元损伤。为解决这一难题,本研究创新性地构建了一种合成吞噬凋亡受体(SER),其整合了针对Aβ的单链可变片段抗体、基于TIM4的吞噬受体框架以及用于小胶质细胞(MG)重编程的下游信号模块,从而实现选择性清除Aβ而不诱导炎症反应。具体而言,本研究开发了自主设计的小胶质细胞编辑型mRNA脂质纳米颗粒(MERLINs),可高效递送SER mRNA至小胶质细胞,使其在体内原位生成Aβ特异性的SER-MG。体外实验显示,SER-MG具备强效的Aβ特异性吞噬能力,并激活典型的抗炎性吞噬凋亡信号通路。在阿尔茨海默病小鼠模型中,SER在MG中的表达显著增强了Aβ清除效率,抑制了炎症反应,从而改善了行为学表现,并显著减少了突触丢失。研究结果表明,通过SER实现阿尔茨海默病相关异常小胶质细胞的抗炎性重编程,可在体内促进Aβ的高效清除,并展现出在其他炎症相关疾病中拓展应用的潜力。该研究成果近日发表于Science Advances,齐鲁医院神经外科倪石磊、张玉霖,药学院姜新义、陈晨为共同通讯作者;第一临床学院本科生张毅、药学院研究生杨贞梅为共同第一作者。
此外,倪石磊团队以近期公共卫生事件为切入点,强调应把短期应急处置转化为长期治理与科技平台建设。研究团队指出,与其只聚焦某一疾病本身,更应把握由此激发的研发契机,打造以核酸药物为核心的通用平台,这一平台对感染性疾病与肿瘤治疗同样关键。倪石磊团队认为,把核酸药物纳米递送做成通用底盘,既能应对突发感染,也能为肿瘤治疗提供可持续的创新动能。该通讯报道近日发表于Nature,神经外科倪石磊为最后通讯作者。
神经外科倪石磊团队长期致力于中枢神经系统疾病发病机制和精准诊疗的临床转化研究,系列研究成果已在Nature,ScienceAdvances,Nature Communications,PNAS,Advanced Materials,ACS Nano,Advanced Functional Materals,Biomaterials,Neuro-Oncology等期刊发表。上述研究得到了国家自然科学基金、泰山学者特聘专家计划和山东省重大基础研究等项目的资助,同时得到山东省脑功能重构省级重点实验室、山东大学脑与类脑科学研究院等平台的支持。