[本站讯]近日,山东大学齐鲁医院神经外科李刚/薛皓教授团队与山东大学晶体材料研究院刘宏教授、济南大学化学与化学工程学院周伟家教授团队合作研发了多个新型纳米催化平台,通过精准靶向与微环境重编程策略相联合,深度激发抗肿瘤免疫反应以实现胶质母细胞瘤的精准治疗,相关研究成果相继发表在Nature Communications(中科院1区Top期刊,IF:15.7)、Chemical Engineering Journal(中科院1区Top期刊,IF:13.2)和Materials Today Bio(中科院1区Top期刊,IF:10.2)等国际期刊。
胶质母细胞瘤(Glioblastoma, GBM)是成人中最常见且最具侵袭性的原发恶性脑肿瘤,免疫疗法已在许多癌症治疗中取得了较好的效果,但因为GBM的高度异质性和抑制性的免疫微环境,其疗效受到了极大的限制。新兴的光动力疗法(PDT)、声动力疗法(SDT)因能直接杀伤肿瘤并激发免疫反应,被视为增强免疫治疗的新方法。然而,GBM微环境的严重缺氧特性极大地削弱了PDT/SDT与免疫疗法的协同效果,如何开发能够克服这些障碍并重塑肿瘤微环境以增强联合治疗效果的新策略,已成为当前该领域的研究热点和难点。
研究成果1:Bioengineered hybrid dual-targeting nanoparticles reprogram the tumour microenvironment for deep glioblastoma photodynamic therapy
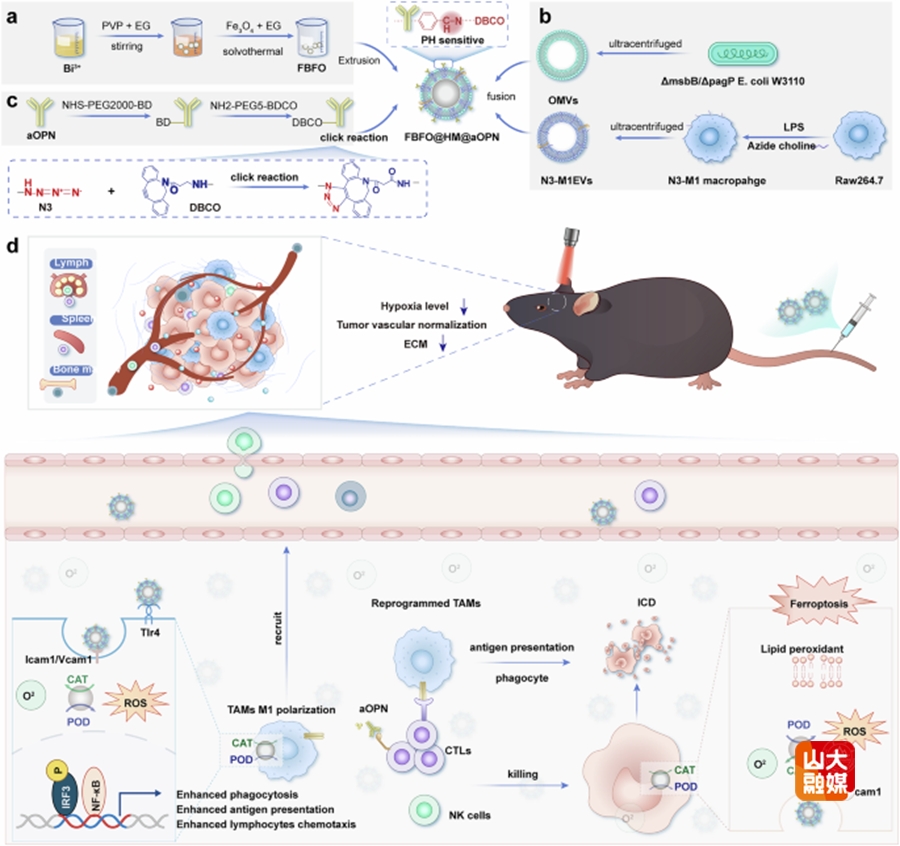
GBM的治疗因其缺氧、免疫抑制的肿瘤微环境及血脑屏障的阻隔而面临巨大挑战,限制了光动力—免疫联合疗法的应用。为克服这一难题,本研究开发了一种生物工程化的多功能智能纳米平台(FBFO@HM@aOPN),用于提高胶质母细胞瘤的疗效。首先,利用具有类过氧化氢酶与类过氧化物酶双重活性的纳米酶(FBFO)构建核心,以缓解肿瘤缺氧并增强光动力效应。随后,该平台被包裹在由M1型巨噬细胞外囊泡与细菌外膜融合形成的“原核—真核”杂交生物膜(HM)中,并进一步修饰了pH敏感的抗骨桥蛋白(aOPN)抗体。进入脑部肿瘤微环境后,纳米平台响应酸性环境释放aOPN抗体,可重塑细胞外基质并增加药物渗透。该体系不仅通过诱导肿瘤细胞发生免疫原性铁死亡来释放肿瘤抗原,还将促癌的M2型巨噬细胞重编程为抗癌的M1型,协同激活了强大的先天性与适应性抗肿瘤免疫反应。研究表明,该策略显著增强了光动力—免疫联合治疗的效果,有效抑制了GBM的恶性进展,并在联合PD-1抑制剂后有效延缓了肿瘤术后复发。该研究从重塑肿瘤微环境以增强光动力—免疫联合治疗这一全新视角出发,为开发高效、精准的GBM治疗方案开辟了新途径。该研究成果近日发表于Nature Communications,李刚教授、薛皓教授、刘宏教授、周伟家教授为论文共同通讯作者;山东大学齐鲁医院神经外科博士后赵荣荣,济南大学博士研究生侯莹,山东大学齐鲁医院神经外科博士后李柏延、潘孜文为论文共同第一作者;山东大学齐鲁医院为第一作者和通讯作者单位。
研究成果2:Biomimetic Hybrid Vesicle Nanoplatform with Pt-BaTiO3for Sonodynamic-Immunotherapy of Glioblastoma
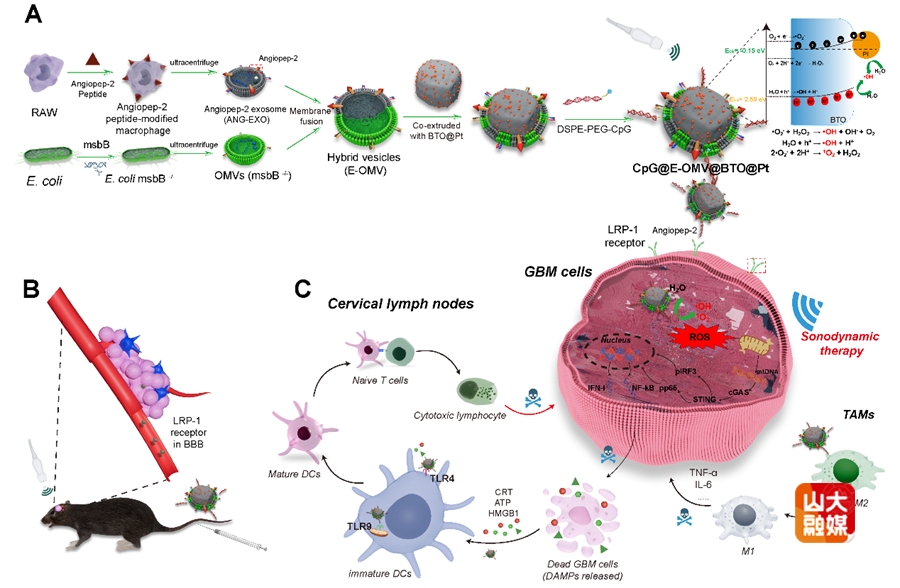
由于多种化疗和靶向药物无法穿透血脑屏障(BBB),使得GBM的疗效受到很大影响。作为一种无创治疗方式,声动力疗法(SDT)凭借优越的组织穿透深度与能量聚焦能力,在脑肿瘤治疗中具有显著优势。本研究构建了杂交膜仿生的声动力纳米平台(CpG@E-OMV@BTO@Pt),用于GBM的免疫治疗与靶向重塑。该平台以 BTO@Pt 为声敏核心,在超声作用下高效产生活性氧,直接杀伤肿瘤细胞并诱导免疫原性细胞死亡(ICD);外层由工程化外泌体与细菌外膜囊泡融合形成 E-OMV 杂交囊泡,既提供脑靶向与免疫伪装,又赋予天然免疫佐剂作用与巨噬细胞重编程能力,从而提升稳定性与递送效率;进一步负载的免疫佐剂 CpG 寡脱氧核苷酸(ODN)可协同促进树突状细胞(DC)成熟,激活适应性免疫应答。本研究以“跨 BBB 精准递送 + 深部声动力催化 + 免疫微环境重塑”为核心策略,为 GBM 的肿瘤纳米治疗提供了可转化的新路径。相关成果发表于Chemical Engineering Journal,李刚教授、薛皓教授、刘宏教授、周伟家教授为论文共同通讯作者;山东大学齐鲁医院神经外科博士后李柏延、济南大学副教授赵莉莉、山东大学齐鲁医院神经外科博士后韩哲为论文共同第一作者;山东大学齐鲁医院为第一作者和通讯作者单位。
研究成果3:Engineering exosome membrane disguised thermal responsive system for targeted drug delivery and controlled release across the blood-brain barrier
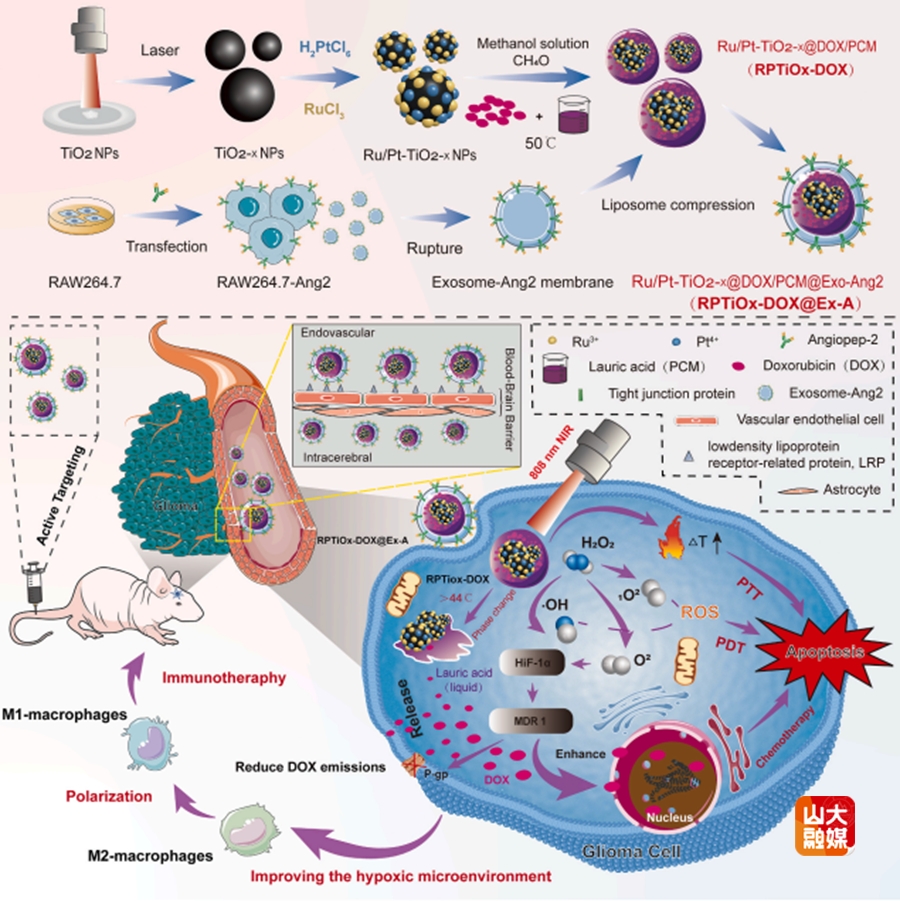
血脑屏障的存在是脑胶质瘤化疗抵抗的重要原因,同时由于肿瘤内血管系统不完善,实体瘤通常会迅速增殖并超过其血液供应,使局部区域处于缺氧微环境中,从而影响外排相关蛋白的表达而进一步增加化疗耐药。针对该项难题,团队设计了一种工程化外泌体膜仿生的热响应复合纳米载药体系,该体系巧妙结合了外泌体膜的生物相容性与纳米颗粒的高效药物传递特性。通过热响应机制,该体系能够在相对安全的温度下释放药物,从而提高治疗的靶向性和安全性。与此同时,针对巨噬细胞外泌体膜的工程化改造,进一步提升了其穿透BBB并靶向GBM的能力,确保了纳米载药颗粒能够高效、精准地递送至肿瘤区域。最终通过“热疗释放药物→催化产氧增敏→免疫强化杀伤”的自增强闭环,为胶质瘤的多模态治疗策略提供了新的思路和方法。该研究成果近日发表于Materials Today Bio,李刚教授、薛皓教授、刘宏教授、周伟家教授为论文共同通讯作者;山东大学齐鲁医院神经外科博士后韩哲、济南大学博士研究生黄海娜为论文共同第一作者;山东大学齐鲁医院为第一作者和通讯作者单位。
李刚/薛皓教授团队长期致力于脑胶质瘤免疫微环境形成机制、关键分子标志物鉴定和精准诊疗的临床转化研究,系列研究成果已在Nature materials、Cancer communications、Molecular Cancer、Neuro-oncology、Advanced Science、Acs Nano、Cancer Res等学术期刊上发表。近年来,李刚/薛皓教授团队与山东大学等多个高水平的研究团队合作,利用医工交叉的手段在脑肿瘤基础研究及临床转化领域取得系列成果,部分研究成果已得到临床验证并在省内多家大型医院推广应用。上述研究得到了国家自然科学基金、科技部重大专项、泰山学者攀登计划和泰山学者青年专家计划等项目的资助,同时得到山东省脑功能重构省级重点实验室、山东大学脑与类脑科学研究院等平台的支持。