[本站讯]近日,山东大学齐鲁医院康复医学科王永慧教授团队在国际权威期刊Neuroscience and Biobehavioral Reviews(中科院一区TOP期刊,5年IF=9.3)发表题为“The anterior cingulate cortex as an integrative hub: Mechanisms underlying pain and anxiety comorbidity”的综述论文。该综述创新性地提出,前扣带皮层(ACC)作为关键整合枢纽,其功能可塑性失调构成了疼痛与焦虑共病的核心神经机制,这一框架性突破为深入理解共病本质、开发协同治疗策略指明了新方向。王永慧教授为本文通讯作者,山东大学齐鲁医院为第一作者和通讯作者单位。

该综述首次系统提出ACC作为多模态信息整合枢纽,其“高增益”可塑性状态是疼痛与焦虑共病的关键神经基础。文章突破了传统上将疼痛与焦虑分开研究的局限,从宏观影像、突触重塑、神经免疫、表观遗传及环路动态等层面,构建了ACC功能失调驱动共病的整合性理论框架。基于这一机制,文章进一步梳理了靶向兴奋-抑制平衡、神经免疫与表观遗传的精准药物策略,以及闭环深部脑刺激、细胞类型特异性调控、聚焦超声等新型神经调控技术的转化前景,为共病治疗从“对症”走向“对因”提供了重要理论依据。
1.疼痛与焦虑共病:临床困境与核心问题
慢性疼痛与焦虑障碍高度共病,约40%的慢性疼痛患者同时患有焦虑障碍,两者形成相互加剧的恶性循环。疼痛作为持续应激源,引发过度担忧和回避行为;焦虑则进一步放大疼痛体验,导致患者功能严重受损、自杀风险升高。然而,当前治疗模式将两者分开处理,效果欠佳,甚至可能导致药物依赖。因此,超越传统的症状描述,深入挖掘共病背后的共享神经机制,是开发有效疗法的关键。
2.ACC的整合视角:从宏观影像到微观机制
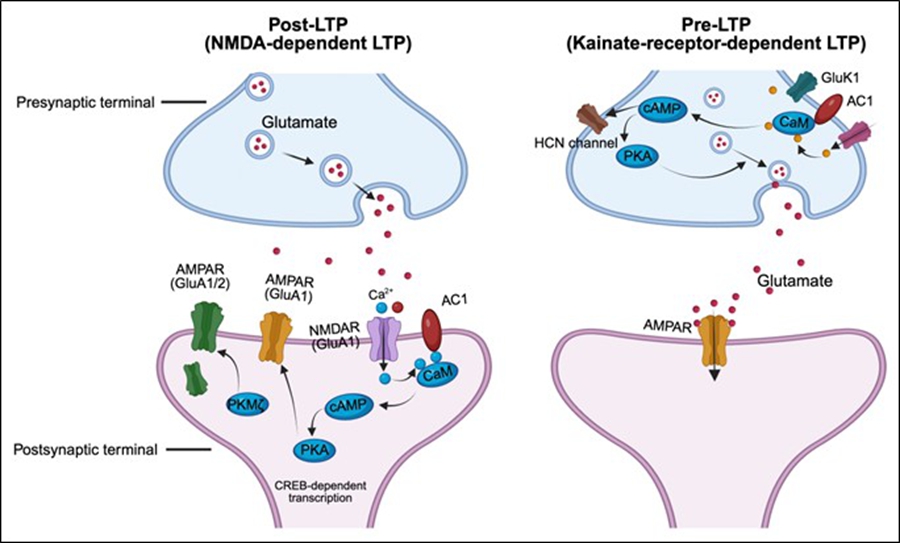
ACC是整合疼痛与焦虑信号的核心枢纽,其功能可塑性异常是疼痛与焦虑共病的核心神经基础。从宏观层面来看,神经影像学证据显示,共病个体的ACC存在异常激活模式、功能连接紊乱以及结构退变。针对ACC的神经调控治疗(如深部脑刺激、经颅磁刺激)可同时缓解疼痛和焦虑症状,进一步证明其因果作用。微观层面,ACC内兴奋性突触传递的长时程增强(LTP)、抑制性控制瓦解、异常的神经免疫相互作用以及表观遗传重编程,共同打破了局部兴奋-抑制平衡。在环路层面,ACC与杏仁核、丘脑、导水管周围灰质以及前额叶等关键脑区之间的动态功能失调。这些多层次机制共同驱动了共病状态的形成与维持。
治疗启示与未来方向
基于ACC机制的治疗策略正不断涌现。药物方面,靶向GluN2B拮抗剂、KCC2激动剂等旨在恢复ACC的兴奋-抑制平衡。免疫调节剂和表观遗传药物也展现出协同治疗潜力。技术方面,闭环深部脑刺激、经颅聚焦超声等神经调控技术可实现精准调控。未来,结合影像、电生理和血生化标志物,有望建立分层医疗体系,针对不同共病亚型实施个性化干预,最终打破“疼痛-焦虑”的恶性循环。
王永慧教授团队长期致力于肌肉疼痛伴焦虑的中枢和外周神经机制研究,系统构建了“外周敏化—脊髓调控—皮层重塑”的慢性疼痛研究体系,揭示了疼痛发生发展的关键分子信号通路、细胞、环路机制,为临床开发精准诊疗方案提供了重要的理论依据和创新靶点。相关研究已取得系列成果,发表于Experimental and Molecular Medicine、British Journal of Anaesthesia等期刊。本研究获山东省泰山学者特聘项目、国家自然科学基金、山东省自然科学基金的资助。