[本站讯]近日,山东大学药学院姜新义教授团队在Nature Biotechnology在线发表题为“A logic-gated trispecific engager enhances macrophage killing of cancer cells in solid tumors”的研究论文。该研究开发了一种逻辑门控三特异性巨噬细胞衔接器,可实现比例性促/抑吞噬信号整合,显著增强巨噬细胞杀瘤能力。姜新义、北京协和医学院邢念增和南京大学张峻峰等为本研究的共同通讯作者。山东大学药学院博士研究生赵晓天、山东大学齐鲁医院荆卫强等为该论文的共同第一作者。
免疫细胞衔接器是一类可桥接免疫细胞与肿瘤细胞并引导免疫细胞定向杀伤肿瘤的新型治疗策略。尽管其在血液肿瘤中已取得显著疗效,但在实体瘤中的应用仍受限于免疫抑制性微环境,尤其是免疫细胞活化不足。巨噬细胞作为实体瘤中高度富集的关键免疫细胞,其吞噬功能依赖促吞噬与抗吞噬信号的动态平衡。现有治疗策略多仅增强或阻断单一信号,难以在巨噬细胞内实现多信号的协同整合,导致激活不足,疗效受限。
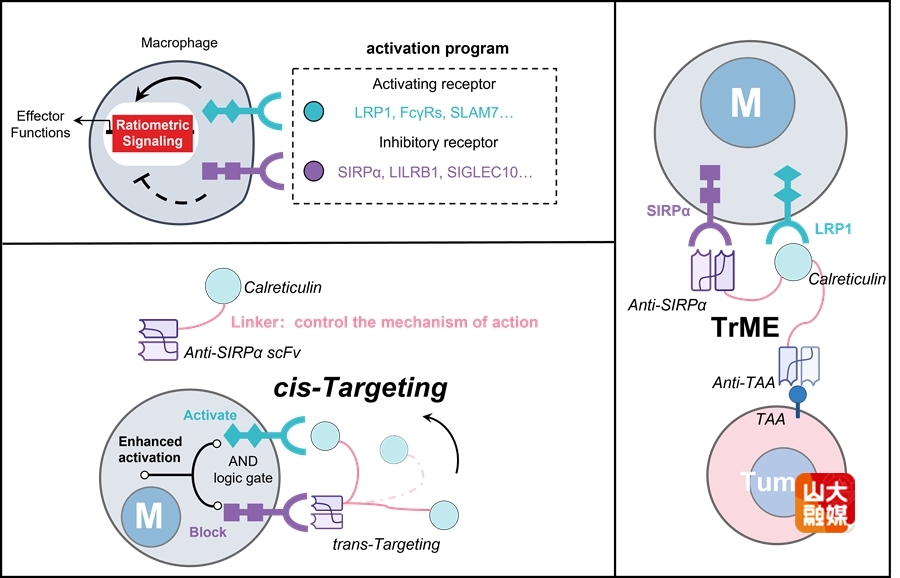
研究团队建立了一种逻辑门控三特异性巨噬细胞连接器(TrME)。该分子基于计算辅助的顺式靶向策略,在巨噬细胞表面同时增强促吞噬受体的活化信号,并抑制抗吞噬受体作用,从而形成“激活+阻断”的AND逻辑门控,实现促吞噬与抗吞噬信号的比例精准调节。TrME在低剂量条件下即可显著提升巨噬细胞吞噬效率,并推动巨噬细胞向促炎表型重塑,整体效能优于早期双特异性抗体。
团队进一步开发了新型LNP体系BCT-A5,显著提升TrME mRNA体内递送效率与蛋白表达持续时间。单次给药即可在肿瘤局部维持持久有效浓度。在胶质母细胞瘤、膀胱癌及乳腺癌等多种原位模型中,TrME均显著抑制肿瘤进展并延长生存期。机制研究显示,TrME不仅增强巨噬细胞吞噬与抗原递呈能力,还促进CD8⁺ T细胞募集与活化,在双侧肿瘤模型中诱导远端肿瘤抑制和表位扩散,体现出先天与适应性免疫协同放大的系统性抗肿瘤效应。
本研究提出了一种基于顺式逻辑门控原理的免疫细胞衔接器构建方案,为突破实体瘤免疫抑制提供了新的治疗思路。该研究工作得到国家重点研发计划、国家自然科学基金等项目的资助。