[本站讯]近日,山东大学微生物改造技术全国重点实验室李盛英教授团队联合中国科学院天津工业生物技术研究所盛翔团队,研究揭示了真菌天然产物中2,2-二甲基-2H-吡喃(DMP)环的生物合成机制,解析了关键氧化还原酶VscB/NotD'介导的“氧化电环化”新反应,为复杂生物碱的高效合成与改造提供了新策略。相关研究结果以“Oxidative Electrocyclization Assembles 2,2-Dimethyl-2H-pyran in Fungal Indole Alkaloids”为题,发表在国际权威期刊《德国应用化学》(Angewandte Chemie International Edition)。山东大学博士生张程杰、硕士生周静旋、天津工业生物技术研究所王伟助理研究员和山东大学博士生刘明钰为论文共同第一作者,李盛英教授、杜磊研究员和盛翔研究员为共同通讯作者。

周环反应(电环化和环加成反应)是化学合成中构建环状结构的重要策略。这类反应也广泛存在于微生物和植物天然产物的生物合成中,参与形成具有复杂结构和多种生物活性的分子。尽管周环反应在化学合成中应用广泛,但自然界中酶催化的周环反应却相对少见,尤其是催化电环化反应的酶学研究极为有限。近二十年来,已鉴定的酶促周环反应主要集中在环加成领域,而电环化反应鲜有报道。
2,2-二甲基-2H-吡喃环(DMP)是众多活性天然产物的核心结构单元,广泛分布于真菌和植物天然产物中。例如:曲霉属和青霉属产生的吲哚生物碱notoamides、芸香科植物中的吲哚酮生物碱,以及藿香蓟植物中的precocenes类化合物。虽然DMP环的化学合成已通过热驱动的全周环反应实现了,但其生物合成机制仍不明确。李盛英团队与合作者前期推测了一些真菌吲哚生物碱(如notoamides、paraherquamides等)生物合成途径中DMP环可能的产生过程,但缺乏直接实验证据,其酶学机制与催化过程亟待解析。

本研究以含DMP环的天然产物versicamide A为研究对象,在杂色曲霉菌DL0022菌株(Av22)中鉴定了其生物合成基因簇,并系统阐明了DMP环的形成机制和所有参与的酶。研究发现,黄素依赖的berberine bridge-like酶(BBE)VscB/NotD'通过氧化电环化反应催化中间体notoamide E的DMP环中关键C−O桥键的形成。
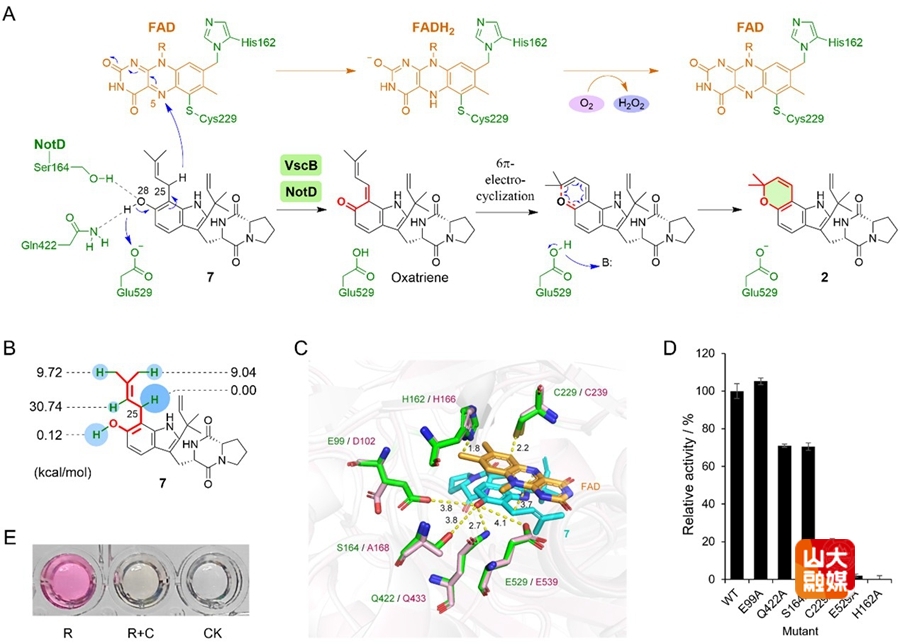
本研究进一步结合结构模拟、分子动力学分析、突变实验及量子化学计算,揭示了该酶的催化机制。结果表明,该反应始于底物向FAD的氢负离子转移。随后,Glu529被底物的酚羟基质子化。而最后环化步骤可能不在酶口袋内发生,更可能是中间体释放到溶液后自发进行。

系统发育树分析表明,VscB/NotD'及其同源酶在真菌界广泛分布,且代表天然产物生物合成中一类新型功能酶。这一发现不仅填补了DMP环生物合成研究的空白,更为开发基于电环化反应的生物催化工具提供了理论支撑。
本研究得到了国家重点研发计划、国家自然科学基金和山东省自然科学基金的支持。