[本站讯]近日,基础医学院高成江教授团队在Cell Death & Differentiation杂志(中科院一区,IF:10.717)在线发表以“TRIM26 positively regulates the inflammatory immune response through K11-linked ubiquitination of TAB1”为题的研究成果。山东大学基础医学院博士研究生赵健和蔡宝珊为论文的共同第一作者,山东大学高成江教授和助理研究员刘冰玉为该论文的共同通讯作者。山东大学为第一作者单位和唯一通讯作者单位。本项研究工作得到了易凡和马春红等教授的支持。
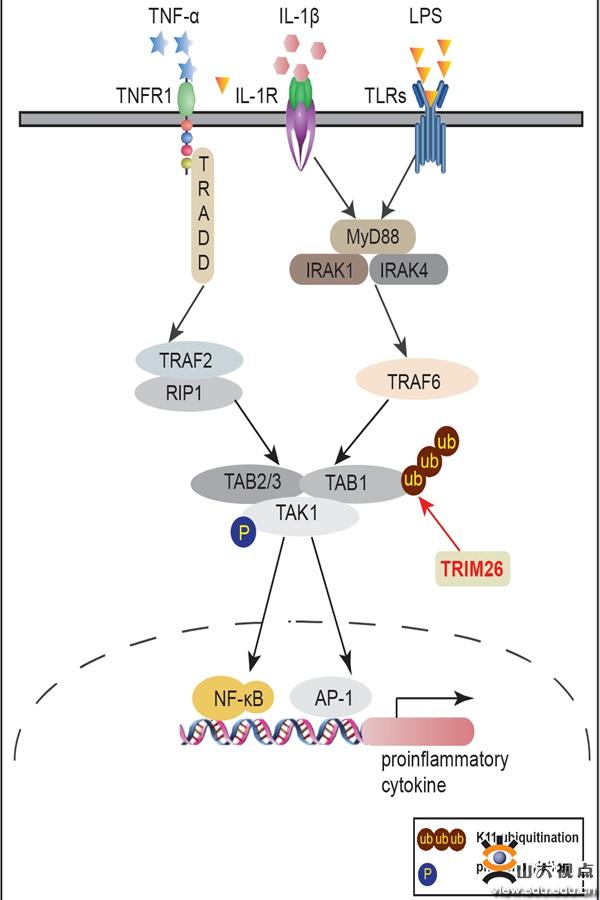
Toll样受体(Toll-like receptors, TLRs)是参与天然免疫的一类重要蛋白质分子,也是连接非特异性免疫和特异性免疫的桥梁。当TLRs被相应配体刺激后,MyD88/TRIF与IRAK1/4等蛋白结合,促进TRAF6及TAK1的激活,并进一步通过NF-κB和MAPK等活化,介导TNFα、IL-6等炎症因子产生,最终在天然免疫抵抗细菌等病原微生物感染过程中发挥着关键作用。TLRs信号的过度激活可导致炎症性疾病,如自身免疫性、内毒素休克、慢性炎症或过敏性疾病。因此,TLRs介导的炎症反应必须得到严格控制。
高成江教授团队已发现泛素连接酶TRIM蛋白家族的TRIM31、TRIM26和TRIM38等成员,在抗病毒天然免疫调控中发挥关键作用(Nat Immunol 2017, 18:214-224; PLoS Pathog 2015, 11:e1004726, J Immunol 2012, 188:5311-5318; J Immunol 2012, 188:2567-2574),但并不清楚TRIM家族成员在炎症反应的功能和作用机制。本研究发现TRIM26在天然免疫TLRs介导的炎症反应中也发挥着关键的调控作用,在小鼠中敲除TRIM26基因可以显著改善LPS介导的内毒素休克。深入的机制研究发现,TRIM26可以与TLRs信号通路下游关键节点蛋白TAB1发生结合,催化其进行K11类型的非经典多聚泛素化修饰,并促进TAK1-TABs复合体的形成及TAK1的激酶活化,最终正向调控TLRs介导的炎症因子生成。该研究揭示了TRIM26介导炎症反应的新机制,并为炎症疾病的治疗提供新的靶点和理论依据。
高成江教授团队长期致力于天然免疫信号转导的调控机制研究,系统探索抗病毒天然免疫信号转导以及炎症反应的调控机制,相关研究成果相继发表在Nature Immunology,Journal of Experimental Medicine,Nature Communications,PLOS Pathogens等国际权威杂志上。上述研究得到山东大学攀登计划创新群体项目、国家自然科学基金重点项目、全国博士后创新人才计划等项目资助。
文章链接:https://www.nature.com/articles/s41418-021-00803-1